随着一系列新药的问世,肺癌诊疗如今已步入慢病化精准管理的时代,对肺癌患者生命长度和生存质量的追求已同等重要,然而新的科学问题也在不断浮现,临床实践面临新挑战。癌肺共病(LCC,Lung Cancer Comorbidities)诊疗这一新理念,正契合当下的肺癌诊疗新格局。《肺癌合并慢性阻塞性肺病(LC-COPD)诊疗国际专家共识》倡导[1],在共病患者治疗中实践“癌肺同治”的理念。针对LC-COPD患者的免疫治疗,需综合考虑肺癌临床分期、病理类型、PS评分和COPD状况。当COPD病情控制处于稳定期时,可行免疫单药或免疫联合治疗,同时密切监测免疫治疗相关不良反应(推荐等级:A;证据水平:2a)。“癌肺共病” 是结合临床实践提出的诊疗新理念。是在全面掌握并整合患者疾病信息的基础上,把复杂医学问题清晰化、条理化、规范化、个体化,以“癌肺共病” 理念为出发点,快速抓住患者诊疗中的主要矛盾再进行综合管理,这将更有利于我们临床工作的高质量开展。

广州医科大学附属第一医院副院长、国家呼吸医学中心临床诊疗部部长、呼吸与危重症学科常务副主任。
在国际上率先提出“重症肺癌”的概念,并牵头发表第一版“重症肺癌国际共识”“肺癌合并COPD诊疗国际共识”
第二届“人民好医生-金山茶花-肺癌领域杰出贡献奖”、第五届“羊城好医生”第一届“广州实力中青年医生”
在我国,肺癌和慢阻肺病是两个严重的公共卫生问题。肺癌患者中慢阻肺病的患病率约为40%~70%,肺癌患者中慢阻肺病诊断率及规范治疗率较低,仅7.1%的患者能够获得准确全面诊断,仅28%~35%患者获得规范化治疗[2-3],诊疗情况不容乐观。
伴肺部合并症(包括合并COPD或肺气肿)的肺癌患者预后更差。一项基于台湾省人群的回顾性队列研究[4]纳入了101776 例肺癌患者,分析了 16 年随访期间肺癌诊断和生存数据,结果显示,伴肺部合并症的肺癌患者总生存(OS)率显著低于未伴肺部合并症患者。此外,相较于其他组织学亚型的患者,鳞癌患者合并症的发生率更高,且在非小细胞肺癌(NSCLC)患者合并COPD患者中,鳞癌与较短OS独立相关[5]。
近年来,随着肺癌的诊断和治疗手段的越来越多样化,化疗、免疫治疗、靶向治疗不断地应用到肺癌治疗领域,肺癌患者带瘤生存以及长期生存不再是“梦想”。尤其是近年来如火如荼的免疫治疗,改变了肺癌患者的治疗模式。
肺癌合并症患者,是否能从免疫治疗中获益?研究发现,肺癌和COPD有着共同的病理生理基础,包括易感基因、免疫异常、慢性炎症损伤和氧化应激等[6]。COPD的慢性炎症会导致细胞因子持续生成,而TGF-β1会诱导Tregs中PD-L1的表达,导致T细胞内免疫失衡和免疫逃逸,这为共病患者接受免疫治疗提供了理论基础。多项研究显示,COPD并不是肺癌患者接受免疫治疗的危险因素[7]。相反,患有COPD的肺癌患者可能相较于无COPD的患者,获得更多收益,包括更佳的 无进展生存期(PFS)、OS和客观缓解率(ORR)[8]。
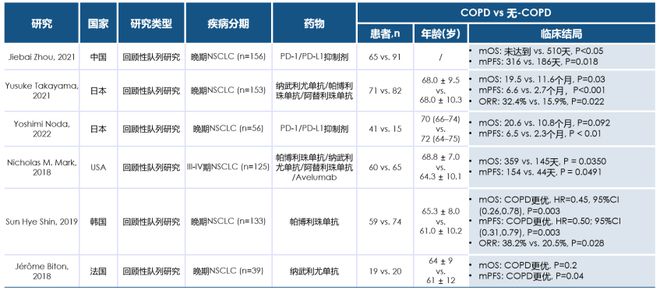
患有COPD的肺癌患者可能比无COPD的肺癌患者获益更多,PFS、OS和ORR均更佳
然而,现实情况是,在伴有合并症的肺癌患者中,免疫治疗的应用比例较低,这其中免疫相关不良事件(irAE)成为了主要治疗难题。相较于肺癌未伴有合并症的患者,Charlson-Deyo合并症评分1或≥2的患者,免疫治疗的使用率显著降低。
肺癌患者在接受免疫治疗时,伴有合并症的整体不良事件(AE)发生率较高。特别是,伴有COPD的肺癌患者,在免疫治疗过程中更容易遭受免疫相关肺炎的困扰。根据2023年免疫检查点抑制剂毒性管理指南[9],高危人群包括:先前患有COPD、肺纤维化、鳞癌、曾接受胸部放疗、正在接受联合治疗的患者,以及现存活动性感染的患者。这些人群在免疫治疗期间需特别关注并防范免疫相关性肺炎的发生。
免疫相关肺炎(CIP)是接受 ICI 治疗的 NSCLC 患者预后不良的严重并发症,研究发现,与无重度CIP的患者相比,有重度CIP(≥3级)患者的中位PFS和OS显著缩短[10]。此外,免疫治疗中的irAE会导致治疗中断,显著影响免疫治疗的疗效。相较于持续的PD-1抑制剂治疗,由于irAE引发的治疗中断,患者的OS较低[11]。
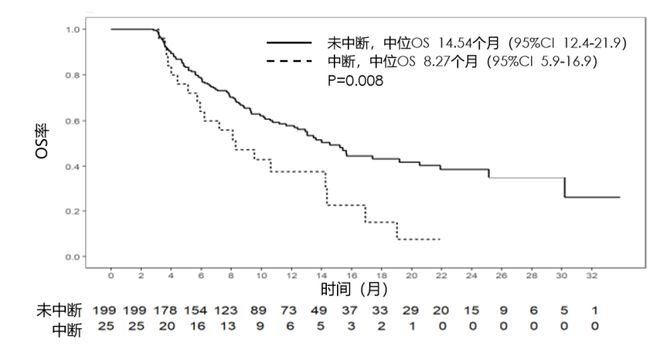
与连续 PD-1抑制剂治疗相比,由于 irAE导致的治疗中断与较低的中位OS 相关
可以看到,肺癌伴合并症患者在寻求免疫治疗药物时,提出了更为严苛的要求。在药物起到疗效的同时,极大的提高了安全性的需求,疗效与安全性如何兼顾成为共病患者治疗的主要矛盾。
PD-L1与PD-1抑制剂的作用机制各异,PD-L1所引发的免疫相关肺炎发生风险相对较低[12] 。PD-1抑制剂能阻断PD-1-PD-L2信号传导,进而增加细胞因子的生成和/或刺激CD4+T细胞的增殖,从而加大CIP的发病率和严重程度。然而,PD-L1抑制剂并不影响PD-L2与其受体PD-1之间的互动,这一特点与肺组织的免疫耐受性密切相关。值得注意的是,RGMb是PD-L2的重要配体之一,PD-1抑制剂可促进PD-L2与RGMb结合。进一步分析PD-L2/RGMb信号通路,我们可以发现:该通路会导致肺内驻留T细胞的剧烈扩增,提升T细胞对自身抗原的活性,破坏肺部的免疫耐受,最终诱导肺炎发生[12]。荟萃分析表明[13],NSCLC中PD-L1抑制剂CIP发生率显著低于PD-1抑制剂。
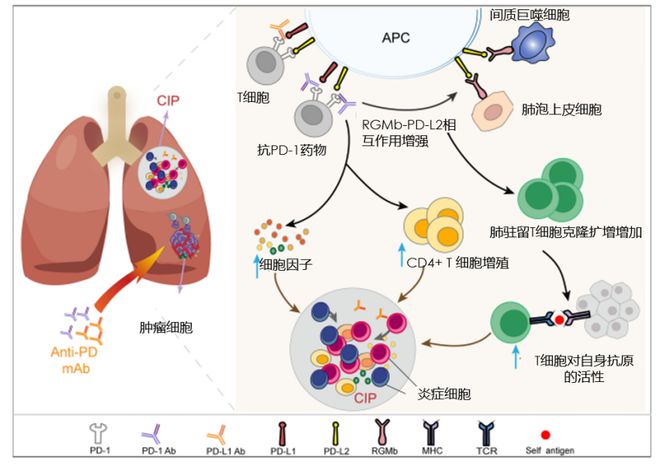
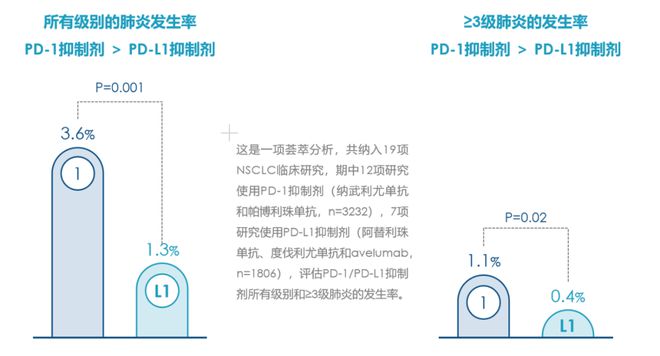
荟萃分析:NSCLC中PD-L1抑制剂CIP发生率显著低于PD-1抑制剂
组成抗体的氨基酸序列全部来自人类的抗体为全人源抗体,相较于其他类型的抗体,其免疫原性较低,从而降低了引发免疫反应的风险。目前的全人源化抗体包括纳武利尤单抗、信迪利单抗、度伐利尤单抗以及舒格利单抗等。其中舒格利单抗是当前医疗领域关注的全长全人源免疫检查点抑制剂。
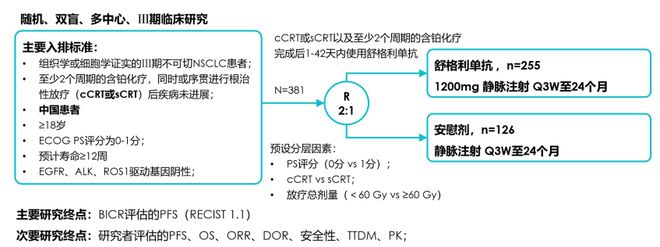
GEMSTONE-301研究[14]是一项Ⅲ期临床试验,纳入了100%的中国Ⅲ期不可切NSCLC患者,研究探讨了同步或序贯放化疗后免疫巩固治疗的疗效。值得注意的是GEMSTONE-301采用了顺序检验,其关键次要终点OS证据级别与主要终点PFS相同。
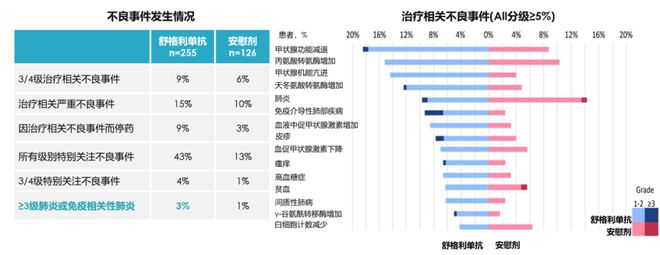
在Ⅲ期不可切NSCLC患者接受同步或序贯放化疗后,舒格利单抗免疫巩固治疗展示出良好的安全性。在巩固治疗两年期间,仅3%的患者发生3级或4级肺炎或免疫相关性肺炎。
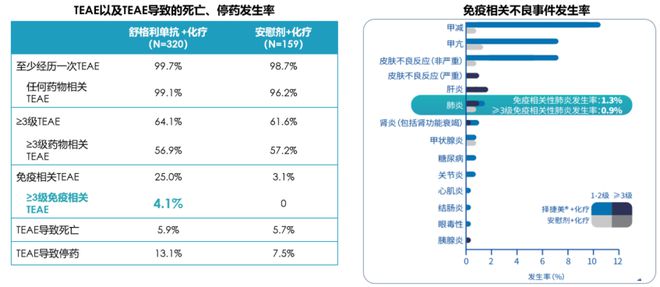
在另一项研究GEMSTONE-302中[15-16],舒格利单抗同样显示了卓越的疗效和良好的安全性。GEMSTONE-302研究是全球首个同时在晚期鳞状和非鳞状NSCLC一线治疗中取得成功的Ⅲ期临床研究。采用舒格利单抗联合化疗一线治疗IV期NSCLC,研究结果显示,≥3级免疫相关不良事件发生率低,仅为4.1%,免疫相关肺炎发生率同样较低,发生率仅为1.3%,≥3级为0.9%。这一突破性成果,为肺癌患者带来了新的希望,尤其是鳞癌合并症患者可以考虑舒格利单抗联合方案。
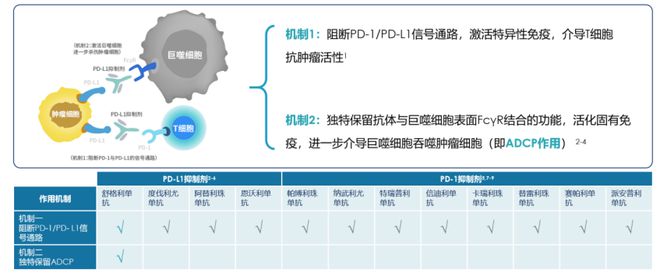
舒格利单抗由于独特的抗体设计,具备独一无二的双重抗肿瘤机制,即通过阻断PD-1/PD-L1信号通道,激活特异性免疫,进而介导T细胞增强抗肿瘤效应。同时独特地保留了抗体与巨噬细胞表面FcγR结合的能力,激发固有免疫,并进一步促使巨噬细胞吞噬肿瘤细胞[14-15,19]。
GEMSTONE-301研究中[14],舒格利单抗巩固治疗展现出显著成效,其巩固治疗显著延长PFS,将疾病进展或死亡风险降低了35%,为患者带来了福音。
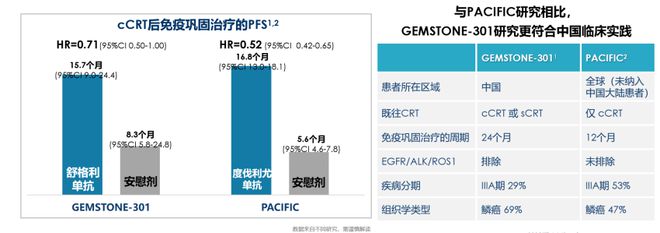
与PACIFIC结果间接来看,GEMSTONE-301研究在年龄≥65岁的患者中,舒格利单抗巩固治疗的PFS-HR(风险比)值更低,展现出卓越的疗效[17-18]。
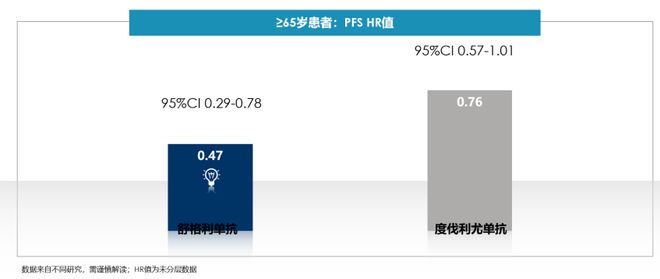
≥65岁患者中舒格利单抗巩固治疗的PFS-HR值更低(非头对头研究请勿直接对比)
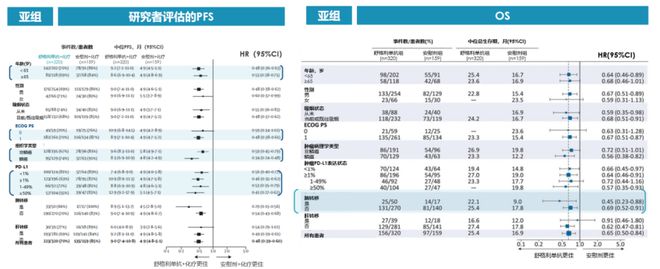
在GEMSTONE-302研究中[15-16],舒格利单抗与化疗的联合应用在延长患者PFS和OS方面均取得了显著成果。在所有预设的亚组中,PFS和OS均显示出一致的获益。在鳞癌患者中,采用舒格利单抗联合化疗的一线治疗方案,患者的mPFS达到8.3个月,HR=0.34;mOS为23.3个月,HR=0.56。这一结果无疑为鳞癌患者带来了新的希望。同样,在非鳞癌患者中,舒格利单抗与化疗的联合治疗也展现出了卓越的效果。患者的mPFS为9.6个月,HR=0.59;mOS为26.9个月,HR=0.72,进一步证实了舒格利单抗在非鳞癌患者治疗中的重要作用。
基于优异的疗效和安全性,CSCO 2023指南I级推荐舒格利单抗用于IV期NSCLC一线治疗,及局部晚期NSCLC同步、序贯放化疗后的免疫巩固治疗。
对于处于COPD控制稳定期的共病患者,在其免疫治疗的选择中,是否PD-L1最终的治疗结果优于PD-1,以及对于疗效及安全性的量化,急需前瞻性研究,提供进一步的证实。
“癌肺共病” 这一新理念的提出,顺应了肺癌进入慢病化管理时代进程的需求。目前对“癌肺共病” 尚存在认知薄弱、诊断不足、病情复杂、治疗难度大、各疾病间潜在相互机制未明等难点。在肺癌患者长生存、高质量的更高要求下,以“癌肺共病” 理念为出发点,快速抓住患者诊疗中的主要矛盾再进行综合管理,以人为本,同诊共治的综合治疗理念亟待推广和践行。
[9]中国临床肿瘤学会. 免疫检查点抑制剂相关的毒性管理指南(2023版). 人民卫生出版社.

