CAR-T生产过程包含多个环节,T细胞分离,富集,激活,病毒载体生产,CAR转导,CAR-T扩增等。每个环节都有一些关键质量属性,对其进行优化,以获得活力最佳、制剂稳定、可用于临床的CAR-T细胞产品。
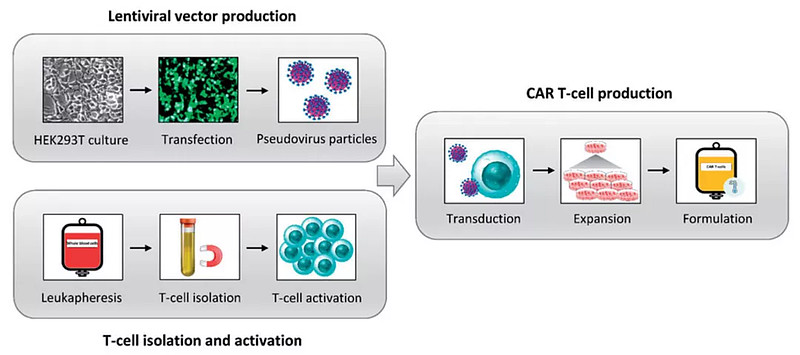
CAR-T生产的每个环节都存在一些变量,这些变量影响CAR-T细胞质量,因而是关键质量属性及优化重点考量点。
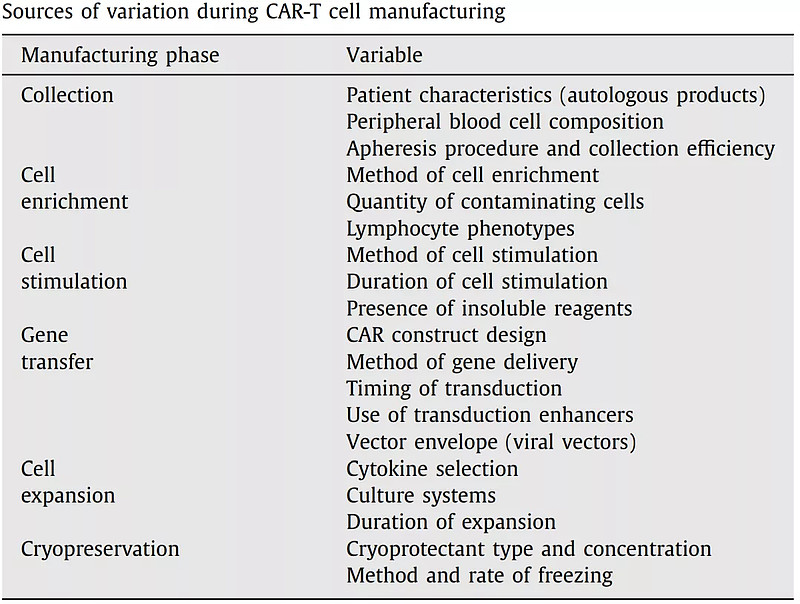
自体单核细胞成分血分离是CAR-T原始材料收集的主要方法。许多患者本身的因素(疾病类型、高龄、前序治疗、外周血特征等)会影响收集细胞的数量和质量。
和健康捐赠者不同,癌症患者通常接受过放疗,化疗等治疗,伴随着淋巴细胞减少症等。比如:与非霍奇金淋巴瘤和慢性淋巴细胞白血病相比,B淋巴细胞白血病(B-ALL)患者的收集效率降低(小于40%)(文献2)。
大多数研究者认为外周血或原材料中NaiveT细胞表型比例越高,则扩增能力越强,持久性越好。而耗竭表型(如表达PD-1,LAG3)的CD8+T细胞比例高,则可能导致治疗失败。
血液成分收集获取细胞初始材料,参数优化以及设备选择,也还在研究之中。比如有研究认为Spectra Optia系统比COBE Spectra系统效率更高(文献3)。
另外不同患者血液参数不同,因而收集所需要的时间也不同,甚至一些低淋巴细胞的患者无法收集到足够的细胞进行细胞治疗。现在开始研究使用健康人群的血液,这样可以收集到足够数量和保障质量的细胞,可以保障完成所有质量属性的表征,但需要克服异体排斥的问题。
成分血分离后,需要进一步富集T细胞。因为红细胞,中性粒细胞等对于T细胞的扩增有一定负面影响。单核细胞数量增加降低T细胞扩增能力,而中性粒细胞的过多降低转导效率。
细胞富集的方法有多种,主要包括清除非淋巴细胞,和分选淋星空体育 星空体育平台巴细胞两大类。其中抗体磁珠等分选淋巴细胞的方法,除了能够分选T细胞,还可以分选T细胞亚群,比如可以分选CD4+T细胞和CD8+T细胞,然后1:1混合(CD4+T细胞可以辅助CD8+T细胞活化),保障最终产品中二者比例的一致性。
清除非淋巴细胞(如髓系细胞等)的方法,成本更低,但是细胞产品中会包含更多的杂细胞,影响产品的一致性和疗效的一致性。
单细胞富集法无疑成本最高,还没有大量证据显示其优于其他方法。但是在某些情况下,如CD19CAR-T生产中,一些B淋巴细胞白血病细胞被转导,不但会掩盖靶点引起耐药,而且产生CAR-B细胞白血病。单细胞富集法可能在一定程度上,可以避免CAR-T产品中的异常转导细胞(文献5)。
在细胞分选富集后,使用多克隆的、抗原非依赖T细胞刺激来促进T细胞扩增,从而获得足以治疗患者的T细胞剂量。随着T细胞治疗领域的扩大,GMP级试剂正迅速可用于临床产品。
现在有许多不同类型的刺激剂,但需要进一步的研究来确定它们之间的差异和它们可能引起的下游效应。比如有些刺激剂可以诱导强的扩增,但是细胞分化表型更明显,持久性差。基于细胞和基于磁珠的人工抗原呈递细胞可以有效地模拟先天抗原呈递细胞的T细胞激活效应。基于抗体的刺激方法也很常用,它需要通过CD3和共刺激信号来激活,以产生实质性的扩增。
T细胞被激活的天数也需要仔细考虑。有研究者发现,CliniMACS Prodigy (Miltenyi Biotec)刺激时间从3天延长到5天时,细胞生存能力、倍数扩增、CD3%和转导效率均降低。
CAR-T生产,基因转导会引入变异性,对于产品关键质量属性产生影响。常用的载体包括病毒和非病毒两大类,前者转染效率更高,后者安全性更好。
临床CAR-T细胞试验主要采用了基于病毒转导的方法,其中包括使用γ-逆转录病毒和慢病毒载体。γ-逆转录病毒载体是第一个用于制造CAR-T细胞的病毒载体,并受益于高转导效率。慢病毒载体则有低插入风险,安全性更好。
然而,符合GMP的病毒载体生产成本高昂,一些替代方法也在试验中,睡美人转座系统,已经开始进入临床研究,此外CRISPR/Cas9也是一个热门的方向。
当病毒载体被用于产生CAR-T细胞时,转导相关变量包括转导的时间和转导增强子的使用。载体转导可以在细胞刺激期间或在细胞刺激后的几天内进行,转导可以进行过多次。增加载体和T细胞接触的方法,如离心接种等,可以增加转导效率。化学增强剂包括polybrene和重组纤维连接蛋白(Takara),用于促进病毒颗粒和T细胞的共定位。
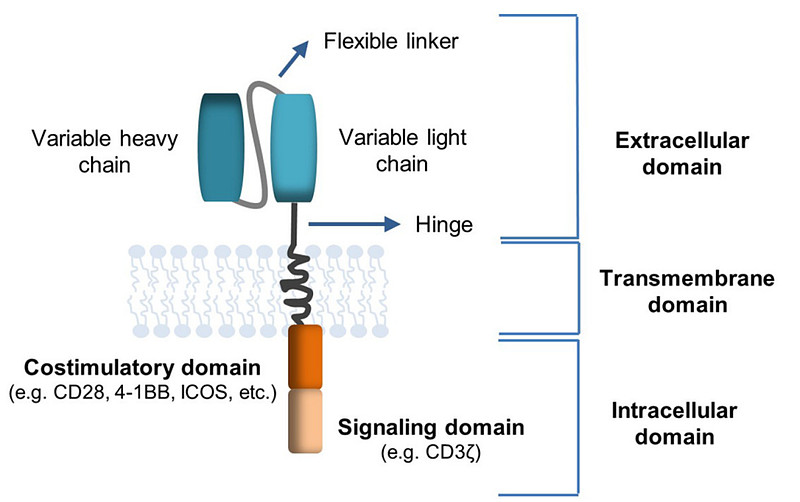
CAR结构也有显著的变异性,它通常由一个细胞外靶点结合结构域、一个铰链区域、一个跨膜结构域和一个或多个细胞内结构域组成。靶点结合结构域被设计用来识别肿瘤细胞,可为人源和非人源,人源化减少产生针对CAR的免疫反应。
理想的CAR-T细胞靶点只存在于肿瘤细胞,正常组织细胞不表达,从而可以减少或避免on target、off tumor毒性。铰链区域提供了稳定性,并使结星空体育 星空体育平台构具有灵活性。
常用的共刺激因子CD28和4-1BB,前者导致T细胞激活更快,但T细胞持久性更短。
细胞扩增以达到治疗所需要的剂量。优化的变量包括培养基、培养基添加物、培养持续时间、生物反应器或培养平台。
GMP级T细胞培养基可用于临床CAR-T细胞试验,并通常补充细胞因子以增强体外CAR-T细胞的增殖。1型细胞因子,特别是γ链细胞因子家族的成员,在T细胞的生存、增殖和分化中发挥着关键作用。IL-2一直是用于CAR-T细胞制造的最常见的细胞因子,可以诱导强的T细胞扩增,尽管可能会牺牲分化和失去Naïve T细胞表型。通过调节IL-2浓度,以增加早期记忆细胞数量。
扩增时间是另外一个重要参数,时间过长,产品中终末分化的细胞增多,杀伤能力减弱,时间过短,难以达到治疗用量。
部分和全自动的系统,如CliniMACS Prodigy和Cocoon (Lonza)开始应用,以GMP级的方式,执行从细胞分选、激活、基因转导、扩增和最终收获CAR-T细胞制造的所有功能。封闭系统和一次性材料可以有效地降低微生物污染的风险,以提供更安全的产品,而自动化促进产品的均一性。
生物反应器的选择本身就是制造过程中的一种变量,也会影响最终产品的关键质量属性。
细胞冷冻保存是CAR-T制造过程中的一个可选步骤,可以灵活地安排患者输液时间,以及完成产品放行所需的质控测试。此步骤可在培养开始之前和/或制造最终产品之后执行。从质量的角度来看,这一步是至关重要的,因为不良低温保存会导致细胞丧失、生存能力受损以及细胞表型和功能的改变。
本步骤中的变量包括冷冻介质中冷冻保护剂和添加剂的类型、浓度、冷冻的方法以及储存条件。虽然大多数低温储存使用5%到10%的二甲基亚砜(DMSO)作为低温保护剂,但无DMSO的低温保护剂也在测试中。储存温度通常低于-150℃。
冷冻保存后,PBMC可以解冻以开始培养并制造CAR-T,而最终的CAR-T细胞产品可解冻用于输注。此步骤中引入许多变量,如解冻持续时间和解冻速率。虽然37°C的水浴最常用于解冻细胞治疗产品,但为减少水源性污染风险,干式解冻系统也可用,并有助于提供更安全的产品。
冷冻保存的原料,在解冻并放入培养中时确实会失去活力,特别是在培养开始两天左右。然而,所有培养产物最终恢复并扩增到足以满足临床剂量,最终的CAR-T细胞在活细胞的恢复、转导效率、CD3阳性率和CD4:CD8比率前后没有差异。但有研究显示凋亡分子上调,TCR信号减弱。临床结果不受影响,包括CAR-T峰值及持久性。
放行检测通常参照监管机构颁布的标准检测方法,如果无,则需要建立内部质控标准。

