在体内,患病感染后的幼稚(初始)CD8+T细胞(Naïve CD8+ T cells)会扩增并分化为效应和记忆T细胞,有助于病原体清除并提供长期保护性免疫。在这一现象的基础上,人们开发了过继性CD8+T细胞免疫治疗,即从患者身上分离T细胞,通过基因修饰进行离体工程,并将其输回患者体内。然而,这一疗法的效率不可控,这归因于常常会出现不利的T细胞表型。最近的研究表明,来源于幼稚亚群而非记忆亚群的效应CD8+T细胞在过继免疫治疗中展现出了更为优越的性能。因此,在T细胞幼稚的状态下进行工程设计对发展过继疗法来说具有重要的意义。然而,目前的离体T细胞工程方法需要用CD3/CD28交联抗体和细胞因子进行预激活。这会导致T细胞失去初始的状态;从而降低了其扩展、持续和治疗疾病的能力;并且赋予不抵抗耗尽的分化程序。因此,研究对幼稚的CD8+T细胞编程的方法以在没有事先激活的情况下引发持久的效应器反应是至关重要的。
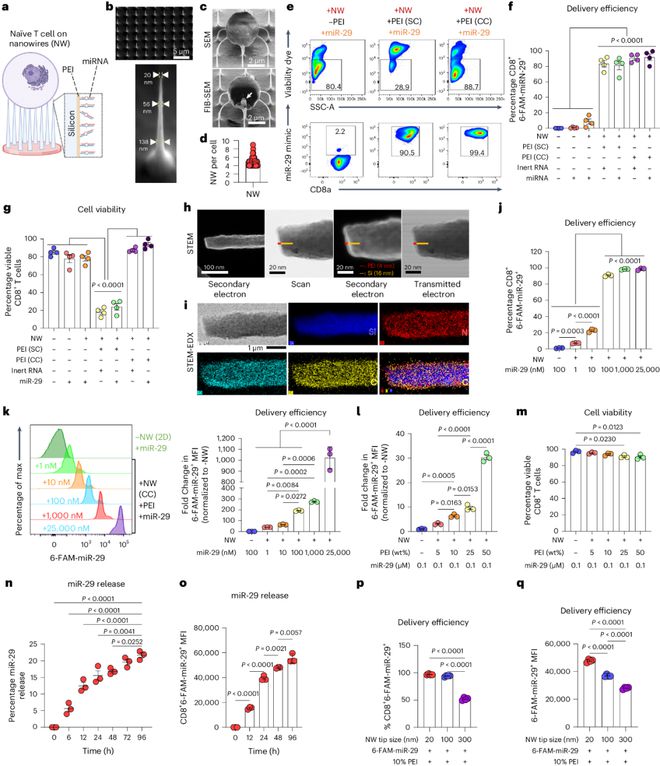
在这项研究中,佐治亚理工学院Ankur Singh教授和康奈尔大学Brian D. Rudd教授等人成功地利用阳离子聚合物功能化的纳米线+T细胞的命运,以实现体内治疗反应。这是通过在没有预激活的情况下向初级幼稚小鼠和人CD8+T细胞递送单个或多个微小RNA(miRNA)来实现的。不仅如此,纳米线的使用还可进一步递送具有长期整合潜力的大的、完整的慢病毒颗粒。研究显示,miR-29和miR-130的缺失和过表达的组合可在幼稚状态影响离体T细胞分化的命运。也就是说,使用纳米线递送的miRNA共递送可对CD8+T细胞进行编程,通过改变T细胞增殖、表型和转录调节以及效应分子的分泌来调节T细胞适应度。此外,通过纳米线介导的miRNA的双重递送编程的小鼠CD8+T细胞的体内过继转移可对不同类型的细胞内病原体(流感和李斯特菌)提供增强的免疫保护作用。体内分析表明,幼稚CD8+T细胞中miR-29和miR-130水平的同时改变降低了典型记忆T细胞的持久性,而增加了短命效应T细胞的数量。因此,这项研究表明,纳米线+T细胞分化,并在不需要预激活的条件下在体内实现治疗反应。相关工作以“Functionalized nanowires for miRNA-mediated therapeutic programming of naïve T cells”为题发表在Nature Nanotechnology。

小的调节性RNA——微小RNA(miRNA)——在T细胞的发育、存活、激活和分化为效应细胞和记忆细胞状态的过程中发挥关键调节因子的作用。抗原刺激后,单个miRNA可对CD8+T细胞的命运产生显著影响。然而,CD8+T细胞分化是一个连续的过程,其中命运决定需要多种miRNA的相互作用。尽管如此,大多数T细胞中的miRNA操作研究都集中在单个miRNA上。在该研究中,作者首先假设多种miRNA的同时调节可以更有效地切换幼稚T细胞的分化开关,并在体内调节T细胞的治疗潜力。从技术上讲,将包括miRNA在内的遗传物质输送到幼稚的T细胞中是极具挑战性的。而将多种miRNA递送到同一幼稚T细胞中进行体内调节更是尚未得到证实。递送miRNA的传统方法涉及电穿孔、慢病毒转导或使用阳离子或脂质体递送系统,这需要用CD3/CD28交联抗体和细胞因子预激活T细胞。预激活可导致某些效应谱系对过继性T细胞治疗无效或导致转导的T细胞耗竭。相反,聚合物纳米技术,如纳米线,可以有效地将生物分子输送到哺乳动物细胞,包括预激活的T细胞。为此,作者设计了垂直的硅基纳米线 nm直径的尖端——可以防止刺穿细胞。该纳米线 纳米线,可形成更宽的尖端和基底,从而有利于生物功能化,包括加载多种miRNA和大病毒颗粒。扫描电子显微镜(SEM)证实,每个CD8+T细胞可与大约有五个纳米线 cm正方形纳米线芯片上播种一百万个T细胞以覆盖900万个纳米线)。随后,作者使用硅烷官能化的N-羟基琥珀酰亚胺(NHS)片段将10wt/v%PEI共价偶联到硅纳米线表面,从而通过静电相互作用增强核酸吸附,同时还能避免由物理吸附表面释放的游离PEI的细胞毒性作用。研究显示,如此装载的miRNA向初级幼稚小鼠CD8+T细胞的递送效率90%,并且T细胞的活力还能保持90%。不仅如此,纳米线还可以增强慢病毒向初级幼稚人类CD8+T细胞的递送。作者用编码慢病毒的eGFP涂覆了PEI功能化的纳米线%的负载效率。这些数据说明,利用纳米线可以向T细胞递送范围非常广泛(小到miRNA,大到慢病毒)的有效载荷。
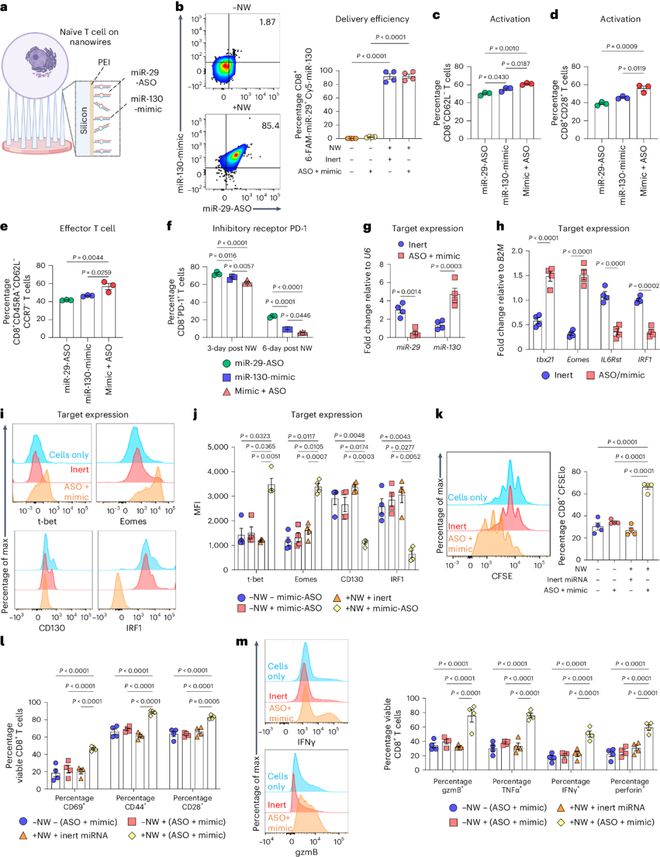
研究显示,纳米线模拟物的递送可以通过下调T-bet和eomes来维持CD8+T细胞的幼稚状态,其中T-bet是促进效应器分化和获得效应器功能的关键CD8+T转录因子,这初步表明了miRNA的递送可在幼稚T细胞中改变靶向基因表达。miR-29在幼稚CD8+T细胞中表现出高表达,而miR-29在T细胞激活时的下调对于有效的细胞杀伤至关重要,缺乏miR-29会表现出对感染的抵抗力;同时,miR-130在T细胞激活后不久z则会上调,促进效应器功能的快速实现。因此,纳米线-拮抗剂(反义寡核苷酸(ASO);减少miR-29)和miR-130-模拟物(增加miR-130)可以在感染前设置激活变阻器(activation rheostat),导致幼稚的CD8+T细胞更快地分化为效应细胞,并偏离细胞的记忆命运。因此,与单个miRNA相比,在用抗CD28/抗CD3珠转染后刺激时,共递送miR-29-ASO和miR-130-模拟物可导致幼稚CD8+T细胞的活化显著更高。与miR-29-ASO相比,单独的miR-130模拟物增加了CD8+CD62L-的百分比和活化的CD8+CD28+T细胞的百分比,而双重递送更是具有相加效应。有趣的是,miR-29-ASO/miR-13 0-模拟物共同递送至幼稚T细胞延迟了抑制性受体程序性细胞死亡蛋白1(PD-1)的表达,防止了衰竭样表型。此外,miR-29-ASO/miR-13 0-模拟物的共递送明显提高了T细胞的增殖能力,增加了细胞溶解分子的产生——穿孔素、颗粒酶B、TNFα和IFNγ(图2)。
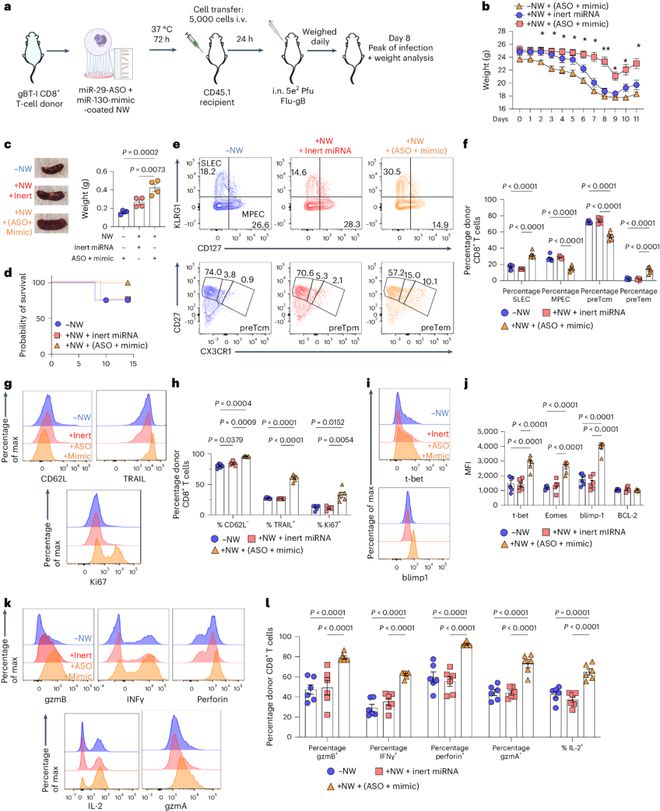
RNA测序(RNA-seq)分析显示,与惰性miRNA相比,纳米线-模拟物共递送调节了幼稚CD8+T细胞的转录组,其中包括与T细胞过程相关的基因上调(例如Eomes、CCL27a和CD59a)或下调(例如Klrk1、Irf1、Ptk2b和Gm11127)。此外,研究也观察到记忆性CD8+T细胞中表达的基因如Pou6f1、Il12b和Il2rb的下调。这其中,Nr4a1(过表达抑制效应T细胞分化)的表达减少,从而可克服T细胞耐受性并增强效应功能。最后,作者用来自转基因C57Bl6/Thy1.1 gBT-I CD45.2小鼠的供体CD8+T细胞进行过继转移实验(该小鼠表达对gB糖蛋白特异性的TCR,并用表达gB肽的重组流感毒株(flu gB)攻击受体)。与对照组相比,接受miR-29-ASO/miR-130-mimic修饰的CD8+T细胞的流感感染受体小鼠的各项生理指标更趋于正常。总的来说,我们的研究结果表明,在急性流感反应中,使用纳米线在初始状态下编程的miR-29-ASO/miR-130模拟修饰的CD8+T细胞表现出更强大的效应器反应,限制了疾病的严重程度(图3)。
本研究证明,纳米线miRNA修饰的幼稚CD8+T细胞在体内初次和二次攻击后能够更好地清除各种细胞内病原体。该研究为纳米线领域增加了新的知识,并解决了T细胞工程中的技术和生物学空白,其中用纳米线递送的多种miRNA可以编程初级幼稚的小鼠和人类CD8+T细胞以提高性能。未来的研究则要着眼于探索纳米线密度对转录组的影响以及miRNA输送到幼稚T细胞胞质室的机制。因此,纳米线能够切换幼稚T细胞的效应器和记忆状态,为新生儿、成人和老年T细胞的免疫学研究开辟了新的途径。
声明:仅代表作者个人观点,作者水平有限,如有不科学之处,请在下方留言指正!
特别声明:以上内容(如有图片或视频亦包括在内)为自媒体平台“网易号”用户上传并发布,本平台仅提供信息存储服务。
崩溃!回上海开了7小时,有人眼睁睁看飞机飞走…这里拥堵达10公里,警方用无人机抓拍喊线
曼城5-1狼队豪取英超6连胜 少赛1场距榜首1分 哈兰德54分钟大四喜
曼城5-1狼队豪取英超6连胜 少赛1场距榜首1分 哈兰德54分钟大四喜
27英寸2K/100Hz仅749元!小米Redmi显示器A27Q 2025款开售
小米双出风立式空调 3 匹预售:1710 m³/h 风量,首发价 5799 元

