众所周知,蝙蝠是一些病毒的天然宿主,其中一些病毒可能蔓延给人类并引起全球性的大流行。与人类不同,蝙蝠可以与高致病性病毒共存而不表现出疾病症状。
作为最重要的第一道防线之一,蝙蝠I型干扰素(IFN-Is)被认为在这种病毒共存过程中发挥了作用,因此近年来受到了广泛的研究。然而,关于蝙蝠是否具有收缩的基因组基因座或组成型表达的IFN,主要是由于物种特异性的发现,存在争议。


作者假设,由于缺乏对所有蝙蝠的全面分析,蝙蝠干扰素I型(IFN-I)的共同特征尚未被揭示。在这项研究中,作者基于高质量的蝙蝠基因组,对九种阳翼手亚目和三种阴翼手亚目的IFN-I基因座进行了表征。此外作者还比较了六种蝙蝠的基础表达,并比较了代表性的菊头蝠干扰素的抗病毒和抗增殖活性以及热稳定性。
为了充分了解蝙蝠的IFN-I系统,作者通过分析基因组位点开始研究。认识到基因组质量对位点注释的影响,只选择了高质量的基因组,包括9只阳翼目蝙蝠、3只阴翼目蝙蝠和8只代表不同进化阶段的非蝙蝠哺乳动物。
研究的第一个观察结果是,在被分析的蝙蝠中有一个一星空体育登录入口 星空体育在线官网般较短的IFN-I基因组位点,而IFN-I基因数量较低。大多数蝙蝠有7-14个IFN基因,唯一的例外是嘴蝠。这个数字低于许多进化上相关的哺乳动物,如牛和猪。
此外,作者还观察到阳翼目和阴翼目蝙蝠之间的显著差异。IFN-I位点通常被一个非IFN基因KLHL9分为两个部分,每个部分中的IFN基因都是独立扩增的。由于所有其他哺乳动物和3只阴翼目蝙蝠都保留了这两个部分,因此9种阳翼目蝙蝠几乎完全失去了KLHL9和IFNb之间的部分。
在所分析的蝙蝠物种中,IFN假基因较少,表明在最初开始时缺乏IFN-I基因的扩增。这意味着蝙蝠似乎选择了一种不同的IFN-I进化路径,以只保留有限数量的基因。
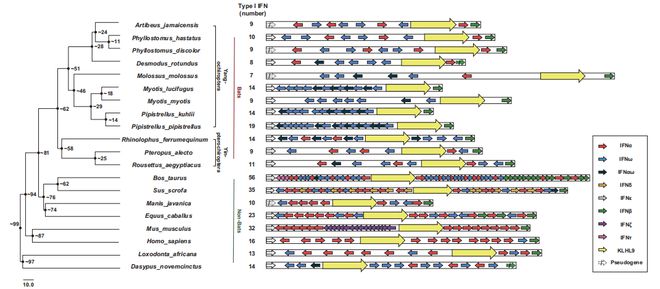
与大多数胎盘哺乳动物选择IFNa而不是IFNw不同,蝙蝠选择了一条不同的进化路径。ifnw样基因主导了蝙蝠的IFN-I位点,这种模式类似于一种相当古老的胎盘哺乳动物。因此,蝙蝠的IFN-I基因座似乎在进化上是古老的。此外,作者发现ifnw样基因在蝙蝠中主导了基础表达。
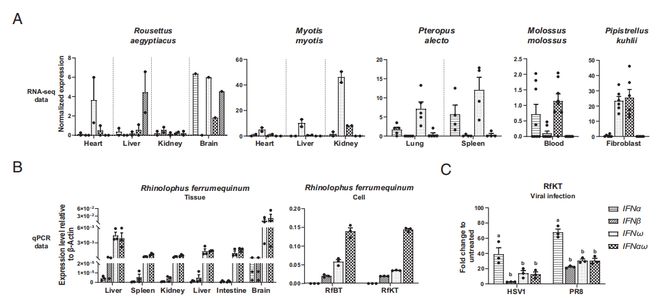
研究人员首先验证了IFNaR1是菊头蝠IFN-Is的功能受体,采用针对病毒RNA的qPCR方法检测病毒的复制水平。所有三种ifn均表现出剂量依赖性和时间依赖的抗病毒活性,IFNaw的活性最高,IFNa蛋白对这两种病毒的抗病毒活性最弱。
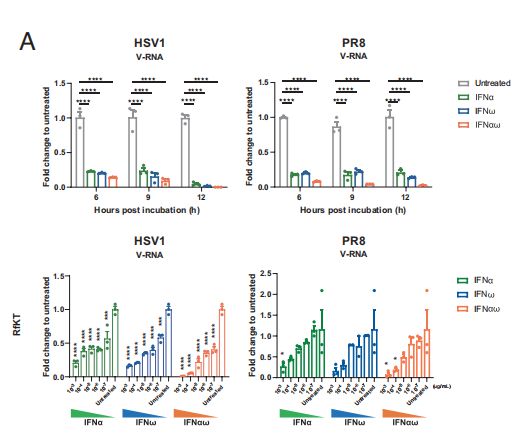
IFNaw蛋白表现出较高的热稳定性和抗增殖活性,IFN-I蛋白的另一个重要功能是抗增殖,这通常与细胞凋亡、组织损伤和抗癌活性有关,IFN-I蛋白的另一个重要功能是抗增殖,这通常与细胞凋亡、组织损伤和抗癌活性有关。总体而言,基础表达的IFNav蛋白不仅在菊头蝠中表现出最好的抗病毒活性,而且表现出最好的抗增殖活性或热稳定性。
总之,研究证实了IFN-I系统中的泛蝙蝠特征,包括基因组位点上IFNw样基因的优势和构成型抗病毒IFNw样反应的优势。这项研究为我们对蝙蝠和病毒之间特殊共存的先天免疫的理解提供了见解。

