经基因工程改造以表达嵌合抗原受体(CARs)的T细胞已在B细胞恶性患者中显示出高效的治疗结果。然而,相当一部分患者仍然对治疗反应不佳或根本没有反应。这其中的主星空体育 星空体育平台要原因,包括T细胞持续性差和T细胞耗竭加重。为此,人们开发了各种遗传工具,以提高抗原识别和信号、维持T细胞干细胞并最大限度地减少T细胞耗竭。这些“细胞内源性(cell-intrinsic)”策略主要集中在合成生物学和T细胞的广泛基因修饰上,以改善和控制其功能。与此相比,细胞外源性(cell-extrinsic)方法展现出了更多的优势,包括更少的制造限制,并可减少对同源T细胞信号网络的潜在有害修饰。
现有的操纵过继转移T细胞治疗活性的细胞外源性方法通常受到了传统疫苗接种或局部递送细胞的启发。也就是说,通过将CAR抗原连接到两亲性配体上,这类两亲性配体运输到淋巴结,然后在那里它们可以刺激CAR活性。此外,编码CAR抗原的RNA纳米疫苗也已用于产生能够刺激外源性CAR-T细胞的抗原。在这两种方法中,抗原被处理并呈递给淋巴器官中的CAR-T细胞,并结合来自内源性抗原呈递细胞(APC;如树突状细胞)的信号,以促进CAR-T细胞增殖和抗肿瘤免疫。然而,在一些患者中,内源性APC只能提供功能失调的共刺激,这限制了它们呈递抗原和刺激T细胞的能力。此外, CAR特异性抗原的全身分布和呈递可能导致临床环境中不可逆、不可预测和不可控制的毒性。
有鉴于此,哈佛大学David J. Mooney教授等人发表研究表明,皮下注射的可生物降解支架有助于特定T细胞亚群的渗透和排出,可形成模拟生理T细胞激活特征的微环境,增强预给药CAR-T细胞的抗肿瘤活性。CAR-T细胞的扩增、分化和细胞毒性是由支架掺入共刺激结合配体和可溶性分子驱动的,并取决于共刺激分子的类型及其出现的环境。在患有侵袭性淋巴瘤的小鼠中,在非治疗性CAR-T细胞给药后,单次局部注射支架可促进产生更持久的记忆样T细胞,并有效延长动物生存期。因此,作者认为,具有优化配体递送功能的可注射生物材料有望提高CAR-T细胞疗法的治疗性能。相关工作以“Subcutaneous biodegradable scaffolds for restimulating the antitumour activity of pre-administered CAR-T cells”为题发表在Nature Biomedical Engineering。

作者假设,设计用于直接原位局部再刺激先前给药的CAR-T细胞的细胞外源性方法可以提高整体系统抗肿瘤活性。此前,作者所在团队已经开发了一种基于生物材料(二氧化硅棒(MSRs))的可注射支架,能够在体外激活T细胞(Nat. Biotechnol. 36, 160–169 (2018))。因此,作者假设这种支架的局部注射变体也可以改变体内系统性T细胞抗肿瘤活性。作者称这些支架为“T细胞增强支架”(TES),可设计用于皮下注射(皮下注射),以形成促进相关T细胞亚群渗透、再刺激和排出的微环境。如图1所示,本研究中的TES就是基于可生物降解的MSRs进行制造的,其负载有T细胞有丝分裂因子白细胞介素-2(IL-2),并涂有由0.1–0.3 mol%的生物素帽磷酸乙醇胺(PE)组成的生物素负载的脂质双层,并且所述生物素帽磷乙醇胺掺杂在1-棕榈酰-2-油酰基-甘油-3-磷酸胆碱(POPC)中。流体双层则提供多克隆T细胞活化配体抗CD3(αCD3)和抗CD28(αCD28),通过生物素-链亲和素连接以促进配体重排的方式连接,以模拟T细胞-APC连接处发生的受体的物理重排。双层上刺激性αCD3和αCD28的摩尔量和比例很容易调节,因此可以改变T细胞再刺激的强度,而支架释放的IL-2模拟T细胞激活过程中的旁分泌信号。
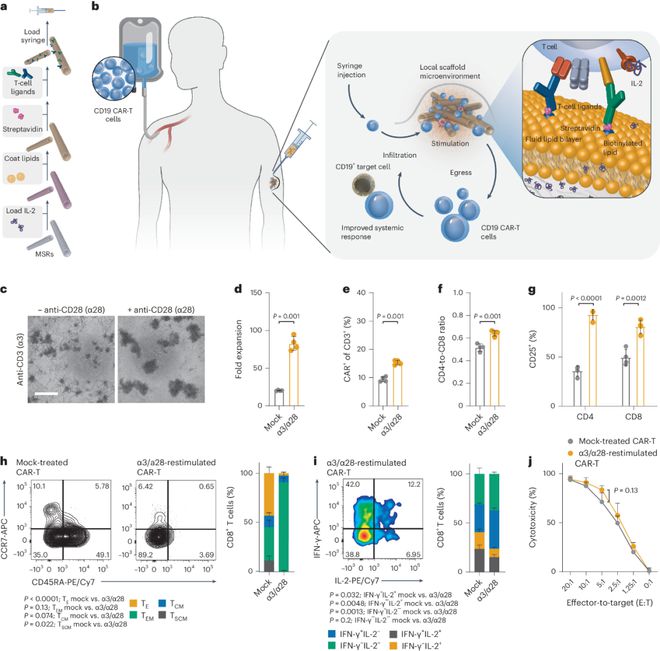
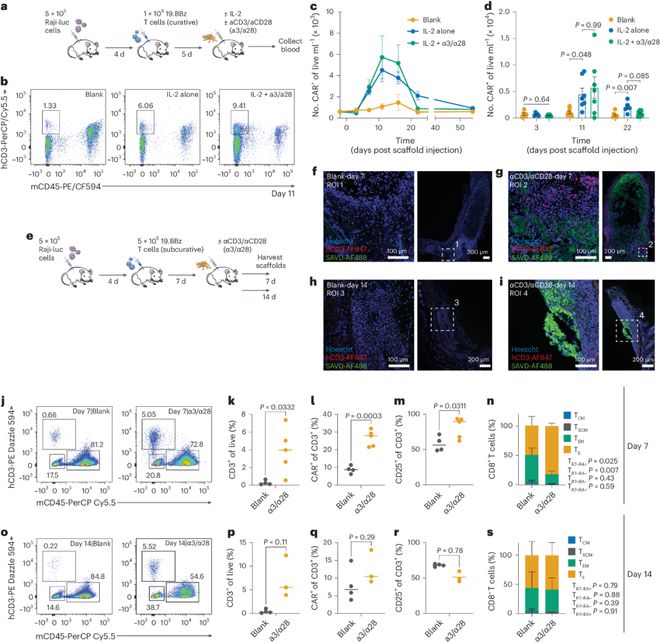
随后,作者制备了CD19导向的CAR-T细胞作为模型系统,以研究上述TES材料的再刺激潜力。通过呈递T细胞活化配体(如抗CD3和抗CD28),发现TES可驱动CAR-T细胞的扩增、分化和细胞毒性活性,从而增强先前在液体肿瘤环境中给予的细胞的全身抗肿瘤活性。作者观察到CAR-T细胞在培养2天后迅速形成大聚集体(与幼稚T细胞中的3-4天相比),这表明来自初始多克隆T细胞激活的残余T细胞信号可能是驱动体内CAR-T细胞下游反应的支持成分。研究星空体育 星空体育平台还观察到,与仅递送IL-2的TES相比,递送αCD3/αCD28和可溶性IL-2的TES促进了循环CAR-T细胞浓度的增加,这可能是由于研究中肿瘤负担减少和高CAR-T细胞输注剂量(1×10 6 CAR-T细胞)所致。在缺乏高肿瘤负荷(因此缺乏连续的全身肿瘤抗原刺激)的情况下,体内CAR-T细胞增殖受到了限制,导致循环CAR-T细胞频率降低,被动渗透到皮下支架中接受αCD3/αCD28再刺激的可能性降低。这表明CAR-T细胞再刺激最有效的治疗窗口期是输注后的初始增殖期(约1周内)(图2)。
研究显示,在高肿瘤负荷条件下,在使用低、非治疗性CAR-T细胞剂量的治疗性异种移植物环境中,单次注射TES能够显著提高动物存活率。IL-2在促进CAR-T细胞增殖和治疗效果方面发挥着重要作用。虽然负载IL-2的皮下支架最初导致动物存活率的适度提高,但作者也观察到从治疗后第34天开始,动物存活率急剧下降。这可能是由于缺乏表面配体和随后的T细胞受体信号传导以及强大的T细胞增殖和分化所需的共刺激所致。另一种可能的解释可能是CD4+T细胞的优先生长,包括Treg亚群30,这可能通过多种机制导致CAR+CD8+T细胞反应受损。鉴于本研究中使用的IL-2水平相对较高,作者预计增加IL-2剂量不会进一步提高TES的疗效。在用TES呈递表面配体处理的动物中还发现了占比更大的循环效应T细胞,这充分表明了递送表面和可溶性活化T细胞配体以直接在体内增强CAR-T细胞反应的可行性和重要性。鉴于表面结合配体的生物利用度限制在约7-14天,作者推测用TES重新刺激的CAR-T细胞的持续治疗益处可能是由记忆亚群的产生驱动的——需要进一步的研究来验证这一点。此外,皮下注射后几个月支架中CAR-T细胞的存在也表明CAR-T细胞可以不断地从支架中渗透和排出,这可能对实体瘤环境的改善具有重要意义(图3)。
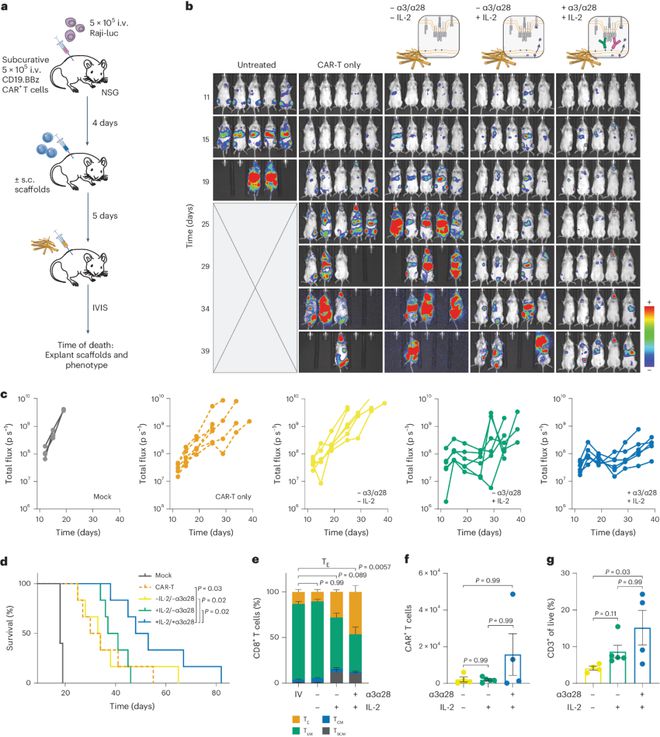
最后,研究指出,未来的工作将关注在实体瘤附近局部注射TES是否也能提高先前给药的CAR-T细胞在实体瘤环境中的有效性。由于实体瘤病变的免疫抑制性质和CAR-T细胞渗透到肿瘤中的难度,在肿瘤病变附近注射的局部皮下支架可以提供更优化的肿瘤反应性T细胞刺激,同时提供所需的生存和增殖信号。因此,作者设想,TES的未来迭代有望提供一种更加经济高效的方法,以本地化和响应的方式提高CAR-T细胞疗法的性能。
声明:仅代表作者个人观点,作者水平有限,如有不科学之处,请在下方留言指正!

