该应用方案中,利用PanT细胞分离试剂盒直接从人PBMC中分离出Pan T细胞,然后用人T细胞活化和扩增试剂盒进行活化和扩增。 流式细胞仪在不同时间点对T细胞纯度、增殖和活化标记表达进行评估。
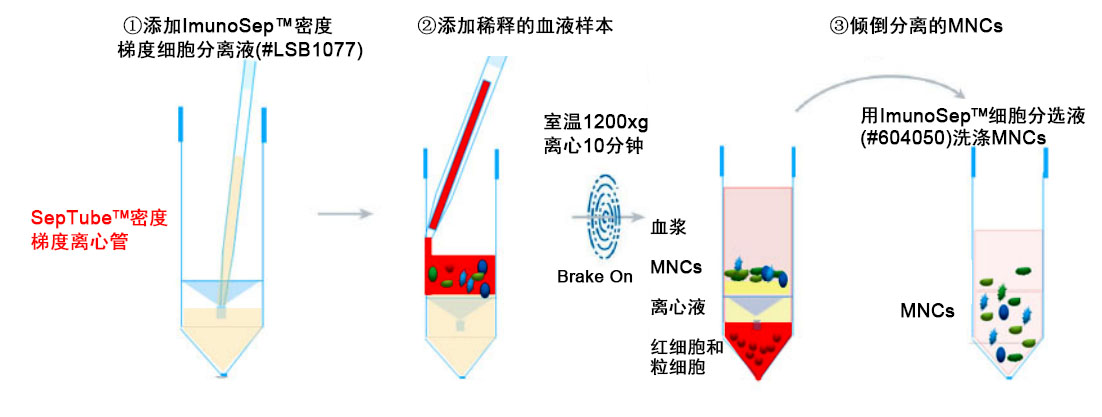
2. 将 ImunoSep™密度梯度细胞分离液(#LSB1077)通过隔板中心的孔注入 SepTube™密度梯度离心管 (如上图 1①)。注入分离液的体积请参考下表。
3. 保持 SepTube™密度梯度离心管垂直,通过血清移液管将稀释的样品沿管壁加入管中(如上图 1②)。 样品将会和隔板上方的分离液混合,但不会影响分离效果。
注:样品也可以直接倒入SepTube™管中,但要小心避免样品通过隔板中央的小孔直接进入隔板下方的分离液中。
4. 水平转子离心机,在开启离心机星空体育官方入口 星空体育官网制动器的情况下,室温1200×g离心10分钟。
注:rpm:每分钟转速;RCF:相对离心力;Radius:离心机转子半径(cm)
5. 离心完成后,将隔板上方包含MNCs和血浆的混合液直接倒入新的离心管中。
注:请勿倒置SepTube™密度梯度离心管超过2秒,以免倒出底层红细胞与粒细胞。
注:离心后,SepTube™密度梯度离心管隔板上表面可能存在少量红细胞,但这些少量的红细胞不会影响下游实验。如果SepTube™密度梯度离心管隔板上表面发现有较多的红细胞,可能是由于采血时间较长引起的,此时可以继续1200×g离心10分钟,以减少红细胞的残留。
6. 在MNCs离心管中添加0.5-1倍体积ImunoSep™细胞分选液(#604050),室温300×g离心8分钟洗涤细胞。
1)SepTube™-15用于处理0.5-5 mL起始血量,SepTube™50用于处理4-17 mL起始血量。
2)SepTube™密度梯度离心管用于从外周血、脐带血或骨髓中分离单个核细胞。血液样品储存时间不超过48h、采血2h内的样品,分离效果较好。
3)如果偶然出现SepTube™隔板插件离心后上浮,请勿倾倒管中的液体收集单个核细胞,此种情况请用无菌镊子移除隔板插件后,再用吸管收集单个核细胞,整个过程操作须小心细致。
4)由于不同疾病状态下的血液与健康人群的血液存在差别,SepTube™分离单个核细胞的效果存在差异属于正常情况,可以根据实际分离情况调整离心时间和血液的稀释倍数,以便取得较好的分离效果。
红细胞压积至少需要0.25 mL。因此对于红细胞比容较低的样本,最小样本体积可能会超过0.5 mL。
红细胞压积的最大体积为3 mL。因此对于红细胞比容很高的样本,最大样本体积可能会少于5 mL。
红细胞压积至少需要2 mL。因此对于红细胞比容较低的样本,最小样本体积可能会超过4 mL。
红细胞压积的最大体积为 12 mL。因此对于红细胞比容很高的样本,最大样本体积可能会少于 17 mL。
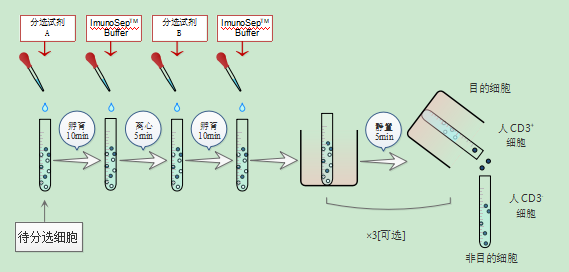
1.用适当体积的ImunoSep™Buffer重悬细胞,调整细胞浓度至1×108/mL(每100μL细胞悬液中含1×107细胞),制备单细胞悬液。
注:细胞必须是单细胞悬液。如有必要,进行涡旋振荡或用移液管移除团块,然后再继续细胞分选。
2. 在12×75mm,5mL流式管中放置所需数量的细胞,但不超过2×108细胞。
3.每100μL细胞添加20μL分选试剂A。通过涡旋仪混匀或利用1 mL Tip吹打5次混匀。在室温下孵育10分钟。
6.每100μL细胞悬液添加20μL分选试剂B,利用1 mL Tip吹打5次或涡旋仪震荡混匀。在室温下孵育10分钟。
注:分选试剂B在添加到细胞悬液前,必须用1mLTip混合均匀,以确保最佳性能。
8.将盛有细胞悬液的5mL流式管插入磁极中,使流式管底部通过磁极底部孔道,直至接触到工作台面。在室温条件下静置5分钟。
9.保持流式管在磁极中,将磁极和流式管一同拿起,快速将上清液倾倒入15 mL无菌离心管中。流式管倒置时长不可超过2秒,随即将其恢复到直立位置。
10.从磁极中取出含有结合CD3+细胞的流式管,再重复步骤7至9,共洗涤3次。
从磁极中取出含有CD3+细胞的流式管,加入1mLImunoSep™Buffer。通过吸取ImunoSep™Buffer来清洗管壁上的CD3+细胞。分选所得的人CD3+细胞可供下游实验使用。
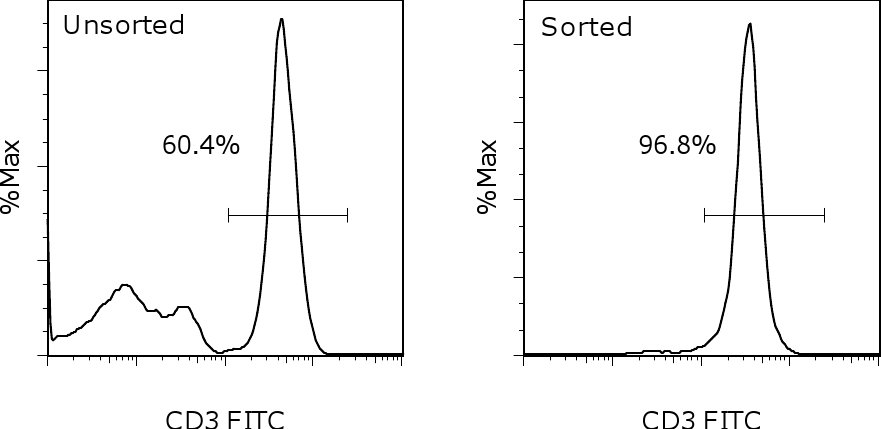
1.将获得的PBMC和T细胞分别悬浮于PBS缓冲液中,制备成1 x 107细胞/mL的单细胞悬液。
2.两支流式管中分别加入50 μLPBMC细胞悬液和50 μL T细胞悬液。
3.将5 μL CD3-FITC抗体混合于流式染色缓冲液中,使检测终体积达到100 μL(例如,50 μL细胞加入50 μL抗体混合液)轻轻涡旋以混合均匀。
5.每支流式管加入2 mL流式细胞缓冲液洗涤细胞。室温400-600xg离心5分钟。弃上清。
注意:一旦重溶,染料应该避光,并在小于或等于-20°C处用干燥剂储存。 建议6个月内使用重溶染料,避免冷冻。
4. 将CFSE添加到所需的最终浓度(例如,对于1μM的最终浓度,每mL细胞加入0.1μL10mM母液)。
注意:可以修改CFSE的浓度、孵育时间和温度,以达到所需的染色强度。 然而,非常高的标记可能导致补偿问题,也可能影响细胞功能。 因此,强烈建议每个研究人员确定最佳测定浓度。
注意:在使用前通过旋涡彻底悬浮抗生物素标记MACS微珠颗粒(包含在T细胞活化扩增试剂盒#中),以获得均匀的悬浮液。
3. 吸取500μL抗生物素MACS微珠颗粒(1×108个抗生物素MACS微珠颗粒),加入到抗体混合物中。
5. 在2-8°c使用MACsmix™管旋转器,转速约为4转/分(最慢的永久运行程序)恒定、温和的旋转下孵育2小时。
6. 负载的抗生物素MACS微珠颗粒(1×106个颗粒/mL)现在可以使用了。 不要从抗体混合物中去除负载的抗生物素MACS微珠颗粒。 储存在2-8°C,长达4个月。
1. 彻底重悬负载的抗生物素MACS微珠颗粒,每2×106细胞加入10个μL(2×106)转移到合适的管中。
2. 加入100-200µL的TexMACS培养基,不需要补充负载的抗生物素微珠颗粒,并在300×g下离心5分钟。
3. 吸出100µL上清液并用添加了IL-2的新鲜TexMACS培养基重悬负载的抗生物素微珠颗粒。
6. 用添加了IL-2的TexMACS培养基稀释细胞使最终浓度为1×106细胞/mL/cm2,并将混合物加入合适的细胞培养容器(例如, 24孔板每孔2×10⁶细胞)
注意:每天检查培养物,如果需要,添加新鲜的添加了IL-2的TexMACS培养基。
9. 将细胞悬液平均分成2份,每份中加入新鲜的培养基,37℃、5-10%CO₂下孵育。
10. 必要时(例如,每2-3天或当细胞达到80%浓度时)将细胞悬液再次平均分成2份,并添加含有IL-2的TexMACS培养基。 在37℃,5-10%CO2孵育。
12. 对于更长时间的扩增,通过每两个细胞添加一个负载的抗生物素微珠颗粒来重新刺激细胞。 接着,计数细胞,每2.5×106/细胞添加12.5μl负载的抗生物素Macs微珠颗粒。
注意:每天观察培养物。 根据扩增率,可能有必要比每2-3天更频繁地分配培养物。
注意:免疫荧光染色不需要去除抗生物素微珠颗粒。 对于在进一步刺激之前需要将T细胞恢复到完全静息状态的检测,抗生物素标记MACS微珠颗粒应在再刺激前至少24小时被去除(见“去除Macsibead颗粒”)。
注意:为了分析T细胞激活,收集刺激48小时的样本并染色早期活化标记CD25和CD69,检测活化的细胞在CD3+细胞中的比例。
注意:高度活化的T细胞一定程度上可能会下调CD3的表达。或者,CD4和CD8染色(例如,带有CD4-VioBlue和CD8-VioGreen)可用于在T细胞亚群的刚刚弄好设门。
注意:较高的温度和/或较长的孵育时间可能导致非特异性细胞标记。在冰上工作需要增加孵育时间。
6. 加入1-2mL的缓冲液洗涤细胞并在300×g下离心细胞10分钟。弃上清。
7. 将细胞重悬悬在适当量的缓冲液中(例如,500µL)用于流式细胞分析。
注意:有些实验(例如,T细胞的再刺激),推荐从细胞悬液中去除MACS微珠颗粒。
1. 将相同处理条件处理的培养孔中的细胞收集在一起。用冷的缓冲液冲洗空培养孔,冲洗培养板上残留的细胞。
7. 将管子仍然置于MACSiMAG 磁极中, 小心移出细胞悬液,转移至新管。

