虽然《中国药典》2020年版收录了两种支原体检测方法,能够灵敏地检测出活的支原体,但是这些方法需要较长的检测时间,对实验室设置和实验室人员的技术要求较高。此外,对于一些特定的样本以及需要快速放行的样本,这些方法也存在一定的局限性,比如针对当前研究热点之一的CAT-T细胞治疗产品的过程或放行检验。因此,越来越多的新兴领域的研发者更倾向于采用支原体污染快速检测方法用于中间品放行检测,甚至作为CAR-T细胞等治疗产品的放行检验的补充或替代方法。

根据物种的不同,支原体可以在液体培养基中生长,可以是单细胞(关节炎支原体),也可以是聚集体(莱氏无胆原体、肺炎支原体、发酵支原体)。由于缺乏细胞壁,支原体对青霉素等针对细胞壁的抗生素具有抗药性。此外,一些支原体可以在液体介质中的固体表面(例如玻璃或塑料表面)上形成生物膜,这提供了另一种水平的抵抗力,即对消毒剂和环境应激条件的抵抗力。
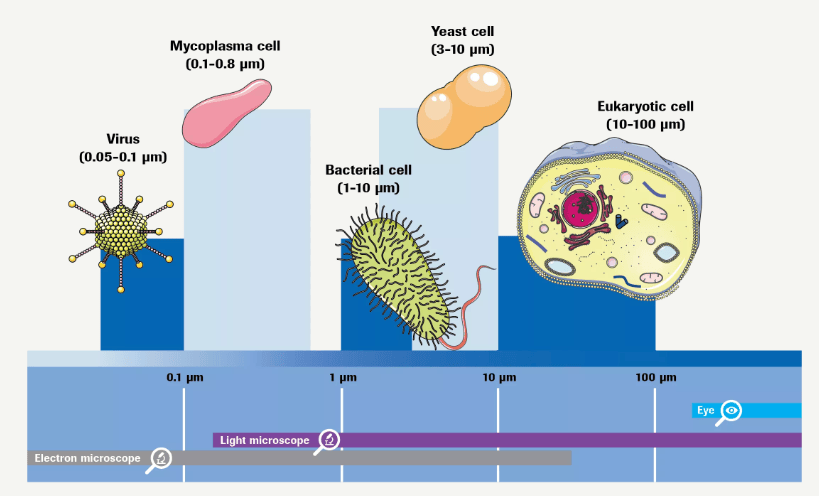
自1956年研究人员首次在细胞培养中发现支原体污染以来,支原体污染的问题就一直广泛存在。生物制品生产过程中使用的动植物源性材料、无机成分、操作环境、操作人员和操作习惯都可能引入支原体污染。各国药品监管机构一直关注支原体污染对生物制品安全性的影响。因此,支原体污染检查成为生物制品外源因子污染检查的重要内容。生物源性原材料和采用细胞培养技术制备的疫苗、抗体、基因治疗产品都需要在生产过程的不同阶段进行支原体污染的检查。
WHO于2010年发布的《生物医药产品生产用动物细胞基质的评价及细胞库检定规程》中首次描述了采用NAT法进行支原体污染检查的要求,”支原体检查的NAT法经过充分的方法学验证并与国家药品监管机构讨论后,单独、与细胞培养法或其它适宜的方法联合使用,有可能会作为一种或两种法定方法的替代方法。这种替代方法需要与法定方法进行可比性研究,包括最星空体育官方入口 星空体育官网低检出限及特异性的可比性。“
2020版中国药典三部《生物制品生产检定用动物细胞基质制备及质量控制》中提出对于生产用细胞,需要对主细胞库(MCB)、工作细胞库(WCB)、生产终末细胞(EOPC)进行支原体检查。
《免疫细胞治疗产品药学研究与评价技术指导原则(试行)》中建议在关键时间点对适合的中间样品开展支原体等安全性相关检测或采取相关的措施加以控制,并且支原体同样需要作为终产品的放行检项。
支原体核酸扩增检测方法(Nucleic Acid Amplification Techniques,NAT)是通过扩增并检测特定的支原体基因组保守序列来进行支原体污染检测的方法,它具有快速、便捷、受样本类型影响小等特点,已成为实验室检测支原体污染的常用方法。
不同的支原体核酸检测方法对支原体的最低检出能力不同,如传统PCR法可检出100~1000变色单位(CCU)的肺炎支原体;降落PCR法可检出10~0.1 CFU·mL -1 的支原体;qPCR法对支原体的最低检出限为10 CFU·mL -1 。针对这些不同原理的方法,目前已有多种商品化试剂盒问世。
支原体NAT法虽然具有快速、灵敏、便捷等特点,但是,由于NAT方法检测支原体的能力依赖于扩增引物序列能否包含足够广泛的常见污染支原体以及在生产中可能通过相关动物源材料所引入的支原体类型,且不同的核酸提取方法、扩增反应体系及扩增程序都可能会对阳性样本的检出效率产生影响。
另外,因NAT方法检出的是支原体的基因组,无法鉴别样品中的支原体是否存活、是否为支原体相近种属的微生物污染、是否存在环境或试剂中的支原体核酸或质粒污染以及是否存在待检细胞核酸或待检样品中其它成分对扩增反应所引起的抑制。

