2025年欧洲肿瘤内科学会亚洲年会(ESMO Asia)已于12月7日在新加坡圆满落幕。本次会议上,肺癌领域亮点纷呈。多项研究在应对表皮生长因子受体酪氨酸激酶抑制剂(EGFR TKI)治疗进展后伴间质上皮细胞转化因子(MET)扩增的难题上取得新发现,勾勒出MET扩增作为耐药机制后的检测、治疗与预后管理全貌。值此,医脉通特邀,深入解读该领域最新研究进展,以期为临床应对此类耐药挑战提供新思路与实践参考。
EGFR突变晚期非小细胞肺癌(NSCLC)一线EGFR-TKI治疗后,MET扩增已成为常见的获得性耐药机制之一,精准识别是后续治疗成功的先决条件。SACHI三期研究已证实,赛沃替尼联合奥希替尼在MET扩增阳性人群中可将中位无进展生存期(PFS)从4.5个月显著延长至8.2个月(HR 0.34,p0.0001)[1],但如何通过可靠检测手段最大化筛选出潜在获益人群,仍是临床亟待解决的关键问题。
本次大会公布的一项研究针对SACHI试验中431例同时接受FISH与NGS检测的患者进行了分析。结果显示FISH总体阳性率约40%,而NGS仅9.9%,敏感性差距显著。一致性高度依赖扩增水平:FISH GCN≥10时,组织NGS阳性符合率升至55%,ctDNA NGS为26%;而在5≤GCN10区间,NGS阳性率星空体育网站 星空体育首页骤降至8.3%和3.3%。这表明NGS,尤其是液体活检,在检测中低水平MET扩增时可能存在显著漏检。更重要的是,55例FISH与NGS双阳性患者中,联合方案PFS达9.59个月 vs 化疗2.89个月(HR 0.26),获益幅度超过整体研究人群,提示高水平MET扩增(FISH GCN≥10)是预测联合治疗方案疗效的关键生物标志物[2]。
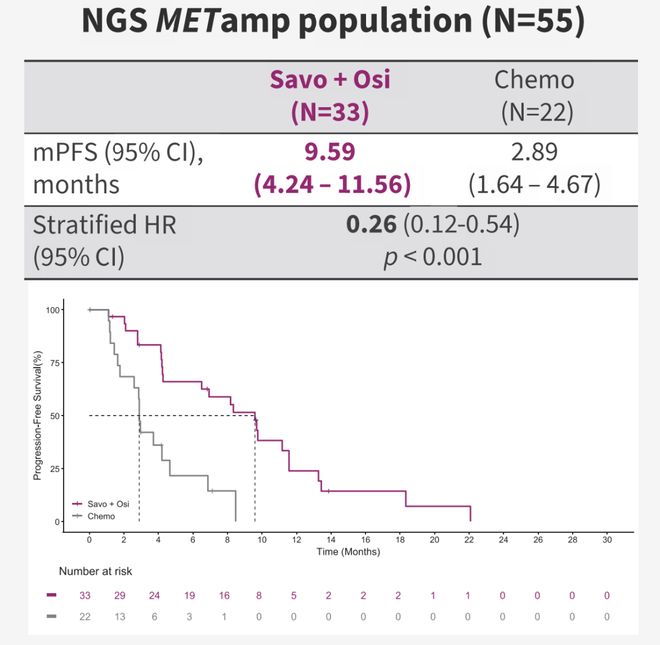
该结果为临床检测路径提供了指引:在EGFR-TKI耐药后MET扩增筛查中,应优先采用FISH并以GCN≥10作为核心判读标准,以避免NGS尤其是液体活检导致的漏诊;NGS虽能发现伴随变异,但单独用于MET扩增判断敏感性不足。事实上,临床共识亦表明FISH是检测MET扩增的金标准[3]。因此,建立“FISH为主、NGS辅助”的规范化检测流程,将有助于真正实现精准人群覆盖,最大化双靶联合的治疗价值。
精准检测的最终目的,是为筛选出的优势人群实现治疗获益的最大化。这种获益不仅体现在肿瘤客观控制上,更应涵盖患者生活质量的维持与改善。SACHI研究最新公布的患者报告结局(PROs)数据显示,联合治疗组在第18周时整体健康状态(GHS)改善或稳定的比例达54.7%,高于化疗组的29.5%(p=0.0003)。在躯体功能、咳嗽、呼吸困难、胸痛、乏力等核心症状的改善或稳定率上,联合治疗组(48.1%-60.4%)也优于化疗组(21.9%-31.4%)。生活质量恶化时间分析进一步显示,联合方案在GHS方面展现出延长趋势(中位TTD:8.312 vs 4.271个月)。此外,在躯体功能、呼吸困难、胸痛等关键指标上,联合方案亦延缓了症状或功能恶化时间[4]。
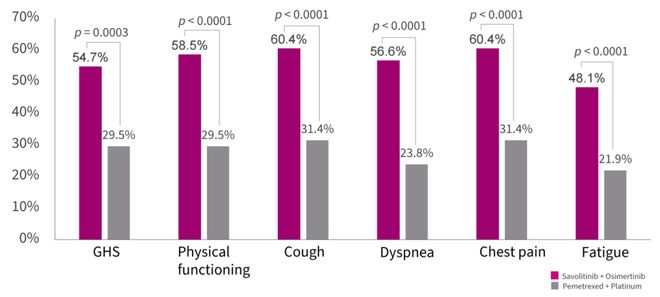
更重要的是,PROs所体现的主观获益与客观疗效指标(如PFS、新发病灶控制时间)呈现高度一致性。这提示对于EGFR-TKI耐药后伴MET扩增这一侵袭性强、预后差的耐药亚群,赛沃替尼联合奥希替尼不仅能有效延长生存,更能维持生活质量。这一从客观疗效到主观感受的全面获益证据链,有力支持该双靶联合方案成为此类耐药患者新的治疗选择。
联合治疗方案所带来的客观与主观获益,必然反映在疾病进展的特征上。理解其具体的进展模式,对于评估治疗的全身控制能力、预测后续治疗窗口至关重要。
SACHI研究的进展模式分析显示,赛沃替尼联合奥希替尼(含化疗组交叉后的合并人群)相较于单纯化疗组,在多个维度上体现出更优的疾病控制效果。首先,在进展构成上,联合治疗组以新病灶出现作为首次进展事件的比例较低(22.5% vs 32.4%),提示该方案能更有效地抑制肿瘤的远处播散。其次,在所有类型的进展事件中,联合治疗组的中位至进展时间(TTP)均呈现数值上的延长。尤其是在控制新发病灶方面,该方案表现出延缓作用:延长了新发脑转移(6.9 vs. 2.8个月)与肺转移(6.9 vs. 3.1个月)的TTP。这一结果不仅印证了联合疗法的全身性疾病控制,更突显了其对中枢神经系统等重要器官转移的延缓作用[5]。
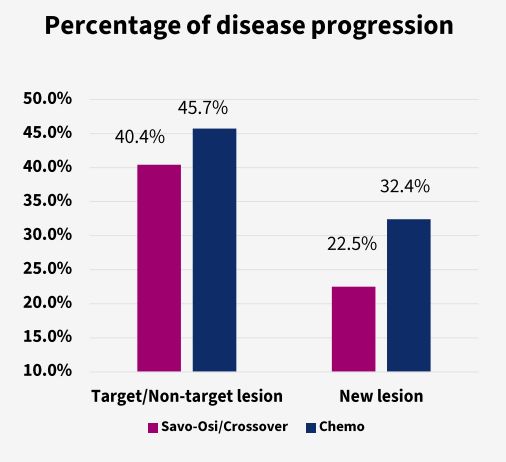
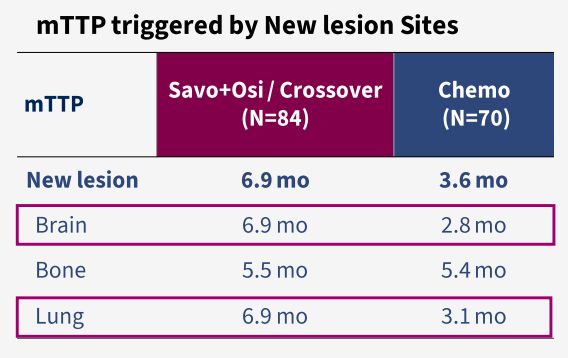
综上所述,这种进展模式的转变提示患者可能获得更长的疾病稳定期和更低的远处转移风险,这使得治疗监测更具针对性,同时也为后续治疗留出了更充分的决策窗口。通过同步抑制EGFR与MET通路,赛沃替尼和奥希替尼联合方案不仅延缓了肿瘤进展,更有望改变耐药肺癌的疾病演进轨迹,为患者带来更深层次的临床获益。
上述研究证据清晰地描绘了理想的治疗路径与获益前景。然而,在真实临床实践中,从“机制明确”到“实际获益”的转化效率如何?一项针对全球13国367例一线奥希替尼治疗进展后伴MET异常NSCLC的真实世界研究揭示了严峻的差距。
该研究显示,获得性MET异常以扩增为主(94%)。MET扩增检测层面过度依赖NGS(77%),而能特异性识别高水平扩增或过表达的FISH(4%)和IHC(10%)使用严重不足,可能导致大量潜在获益患者未被正确识别。在检测结果量化分析中,通过NGS检测显示88%的MET扩增患者基因拷贝数≥6,这为界定临床相关的高水平MET扩增提供了重要依据。治疗选择上,即使在高水平MET异常患者(IHC 3+、NGS GCN ≥6 或 FISH GCN ≥10)中,二线MET-TKI使用率也仅35%,后续线]。
这项分析客观地指出,当前提升MET驱动耐药患者生存的核心矛盾已非缺乏有效药物,而在于检测规范性与治疗及时性的不足。未来亟需通过指南与临床路径优化,大力推广多平台MET检测策略,并强化临床医生对高水平MET异常患者尽早启用靶向联合治疗的意识,从而真正弥合临床研究与真实实践之间的鸿沟,让更多患者从精准治疗中获益。
针对EGFR-TKI耐药后MET扩增的临床管理策略,已经形成了从精准检测到预后管理的完整闭环。当前面临的挑战已从“缺乏有效治疗”转向“如何实现精准人群覆盖与规范治疗”。未来需要临床、病理与检测领域的协同努力,建立以生物标志物为导向的规范化路径,推动检测标准化与治疗精准化的同步提升。这不仅是提升现有患者疗效的关键,更是实现肺癌个体化治疗与全程管理的重要基石。
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。

