的 “免疫红娘” 在默默发力。它作为 CD4+T 细胞的特殊分支,专门帮 B 细胞 “修炼升级”,促成生发中心形成,催生高亲和力抗体,是长效免疫力的关键。本文从 Tfh 细胞的 “身份特质”“工作机制” 说起,拆解它在急性和慢性病毒感染中的不同表现,再揭秘 mRNA 疫苗、纳米疫苗等新技术如何 “讨好” 它来提升防护效果,用通俗的语言带大家看懂这个免疫核心的神奇作用。

说到免疫系统对抗病毒,大家可能会想到抗体、T 细胞这些 “明星选手”,但很少有人知道,背后还有个关键的 “牵线人”——Tfh 细胞(滤泡辅助性 T 细胞)。它就像免疫界的 “金牌红娘”,专门负责帮 B 细胞 “成才”,让抗体变得更强大、更持久。
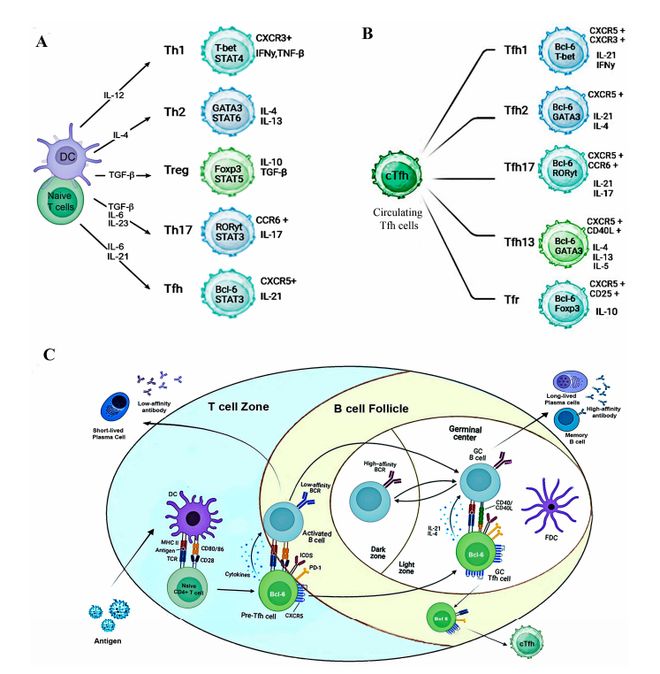
Tfh 细胞是 CD4+T 细胞家族里的 “特长生”,和负责细胞免疫的 Th1 细胞、应对过敏的 Th2 细胞不同,它的唯一使命就是支持体液免疫。要识别它也很简单,它带着几个独特的 “身份标识”:表面有CXCR5(帮它找到 B 细胞的 “导航器”)、PD-1(免疫调节的 “开关”)、ICOS(和 B 细胞互动的 “接头暗号”),还有一个核心的 “指挥者”—— 转录因子Bcl-6,这是它成为 “红娘” 的关键。
它的工作流程特别清晰:先在淋巴结的 T 细胞区被树突状细胞激活,变成 “预备红娘”(前体 Tfh 细胞),然后在IL-21等细胞因子的帮助下,迁移到 B 细胞所在的滤泡区。在这里,它通过CD40L-C星空体育登录入口 星空体育在线官网D40 结合和细胞因子分泌,帮 B 细胞完成 “蜕变”—— 经过体细胞高频突变和类别转换重组,从只能产生低亲和力抗体的 “新手”,变成能分泌高亲和力抗体的 “高手”,还能分化出记忆 B 细胞和长寿浆细胞,让免疫力长期在线。
更神奇的是,Tfh 细胞还有不同 “分工”:负责抗病毒的cTfh1 细胞(分泌 IFN-γ)、应对过敏的 cTfh2 细胞、参与炎症反应的 cTfh17 细胞,它们各司其职,精准匹配不同的免疫需求。还有个叫Tfr 细胞的 “监管员”,会适时调控 Tfh 细胞的活性,避免免疫反应过度。
面对病毒入侵,Tfh 细胞的表现直接决定了免疫反应的 “战斗力”。不同类型的病毒感染,它的应对策略也完全不同。
像流感、寨卡病毒这类急性病毒,来得快、攻势猛,Tfh 细胞会立刻进入 “紧急动员” 模式。在感染后 24-48 小时内,它就开始分化成熟,迅速促成生发中心形成,催生出大量病毒特异性中和抗体。
比如流感感染时,Tfh 细胞分泌的 IL-21 能加速 B 细胞成熟,让抗体快速达到有效浓度;寨卡病毒感染中,它还会变身 “全能选手”—— 兼具 Tfh 和 Th1 细胞的特性,既帮 B 细胞产生中和抗体,又能增强细胞免疫,提供双重保护。研究发现,没有 Tfh 细胞的帮助,针对痘苗病毒的 IgG 抗体产量会暴跌 98%,可见它的重要性。
这种 “速战速决” 的关键,在于病毒带来的持续抗原刺激和 IL-6、IL-21 等细胞因子的协同作用,让 Tfh 细胞能快速分化、高效工作,帮身体在病毒扩散前建立起防护墙。
但面对 HIV、丙肝病毒这类 “持久战” 高手,Tfh 细胞就有点 “力不从心” 了。这些病毒会持续在体内复制,不断刺激免疫系统,导致 Tfh 细胞数量虽然增多,但功能却严重受损。
在慢性感染中,Tfh 细胞分泌 IL-21 的能力下降,无法有效支持 B 细胞产生高质量抗体,甚至会导致 B 细胞 “耗竭”。更麻烦的是,HIV 还会把 Tfh 细胞当成 “藏身之处”—— 因为 Tfh 细胞能躲避 CD8+T 细胞的攻击,成为病毒的潜伏 reservoir,让治疗变得格外困难。
不过也有好消息:慢性感染中,一部分循环 Tfh 细胞(cTfh 细胞)依然保持功能,它们能帮助产生广谱中和抗体,这也成为研发 HIV 疫苗的重要突破口。科学家正在尝试用 PD-1 阻断剂、重组 IL-21 等方法,帮 Tfh 细胞 “恢复体力”,重新发挥作用。
既然 Tfh 细胞是长效免疫力的核心,疫苗研发的核心思路就变成了:如何让疫苗更有效地激活 Tfh 细胞?近年来的疫苗新技术,几乎都在围绕这个目标发力。
减毒活疫苗:模拟真实感染,能提供持续的抗原刺激,是激活 Tfh 细胞的 “王牌”,但安全性风险较高;
灭活疫苗:虽然安全,但免疫原性弱,通常需要加佐剂、打多针才能激活足够的 Tfh 细胞,比如新冠灭活疫苗就通过添加 TLR7/8 激动剂来增强效果;
mRNA 疫苗:这几年的 “明星技术”,凭借脂质纳米颗粒(LNP)的佐剂活性,能高效激活 Tfh 细胞和生发中心反应,产生高水平中和抗体,新冠 mRNA 疫苗就是最好的例子。
mRNA 疫苗的优势在于能精准表达病毒抗原,还能通过 LNP 激活先天免疫,刺激树突状细胞分泌 IL-6 等细胞因子,为 Tfh 细胞分化创造绝佳条件。研究显示,新冠 mRNA 疫苗能诱导强烈的 Tfh 细胞反应,产生的循环 Tfh 细胞能在体内持续存在 6 个月以上,为长期防护提供保障。
除了传统 mRNA 疫苗,自扩增 RNA 疫苗(saRNA)更厉害 —— 它能在细胞内自我复制,持续产生抗原,减少疫苗剂量的同时,还能延长 Tfh 细胞的激活时间,对变异病毒也有更好的交叉保护效果。
这种疫苗用铁蛋白、发光酶合酶等天然蛋白,自组装成和病毒大小相似的纳米颗粒,能多价展示抗原,就像给免疫系统 “递上” 了一个清晰的 “靶子”。它能直接激活 B 细胞,还能通过模式识别受体(PRR)激活树突状细胞,帮 Tfh 细胞更好地发挥作用。
比如铁蛋白纳米疫苗,能在淋巴结的生发中心持续沉积抗原,让 Tfh 细胞和 B 细胞的互动更充分,产生的中和抗体水平比传统疫苗高得多,还能应对病毒变异。
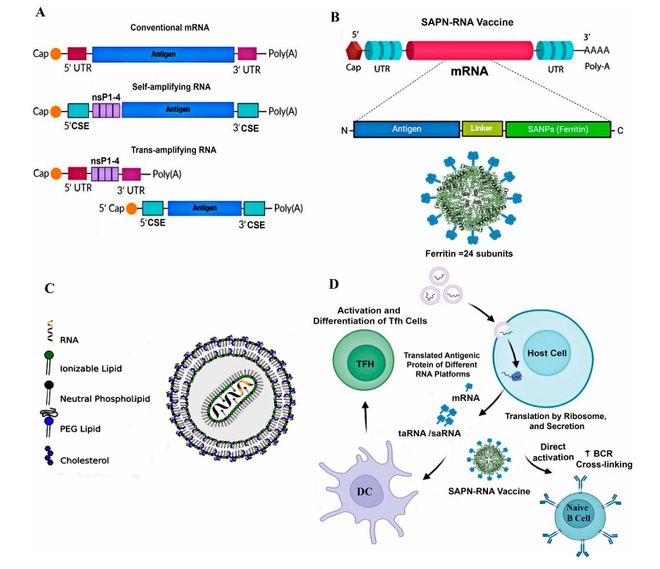
把 mRNA 疫苗和纳米疫苗结合,就是 “王炸组合”——SAPN-RNA 疫苗。它既有 mRNA 疫苗的精准表达优势,又有纳米颗粒的多价抗原展示能力,能直接激活 B 细胞和树突状细胞,让 Tfh 细胞反应更强烈、更持久。研究显示,这种疫苗在更低剂量下就能诱导高水平中和抗体,还能提供广谱保护,是下一代疫苗的重要方向。
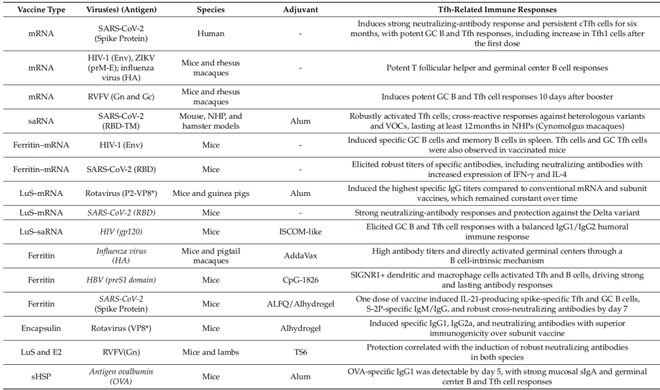
佐剂就像疫苗的 “增效剂”,能帮疫苗更好地激活 Tfh 细胞。常用的铝盐佐剂能诱导 Th2 和 Tfh 细胞反应,但效果有限;而 MF59 等油包水佐剂、TLR 激动剂(如 MPLA、CpG)能通过刺激 IL-6 分泌,促进 Tfh 细胞分化,显著提升疫苗效果。
比如新冠 RBD 疫苗搭配 TLR9 和 STING 激动剂,能让生发中心 Tfh 细胞数量大幅增加,中和抗体水平显著提升;α- 半乳糖神经酰胺(α-GalCer)这类 NKT 细胞佐剂,还能通过激活 NKT 细胞分泌 IL-21,间接帮 Tfh 细胞 “发力”。
虽然 Tfh 细胞的重要性已经明确,但要完全用好它,还有不少挑战:它主要藏在淋巴结等淋巴组织里,很难直接研究;慢性感染中它的功能受损机制还没完全搞清楚;不同物种的 Tfh 细胞标记不同,给兽医疫苗研发带来困难。
不过随着单细胞 RNA 测序、空间转录组等技术的发展,科学家对 Tfh 细胞的认识正在不断深入。未来的疫苗研发会更精准地靶向 Tfh 细胞,比如优化抗原设计、筛选更有效的佐剂、开发多平台联合疫苗等,让疫苗能诱导更强、更持久的体液免疫。
无论是人类疫苗还是动物疫苗,Tfh 细胞都将是核心靶点。相信随着研究的推进,我们会开发出更多能应对变异病毒、提供广谱保护的下一代疫苗,而这一切,都离不开 Tfh 细胞这个 “免疫红娘” 的默默付出。
免疫系统就像一个精密的 “作战系统”,Tfh 细胞虽然不直接 “杀敌”,但它的 “牵线搭桥” 让抗体大军变得更强大、更持久。从 mRNA 疫苗到纳米技术,人类对疫苗的优化,本质上都是在学会如何更好地 “调动” Tfh 细胞。
希望这篇文章能让你看懂这个免疫核心的神奇作用,下次接种疫苗时,也能明白背后还有这样一位 “金牌红娘” 在为你的健康保驾护航~

