CAR-T细胞疗法在血液肿瘤治疗中取得革命性突破,但其在实体肿瘤领域的应用却停滞不前,疗效甚微。究其根本,传统体外扩增的CAR-T细胞在增殖过程中不可避免地伴随分化、耗竭和衰老,导致其难以有效浸润肿瘤组织,即便进入也难以长期存活,成为实体肿瘤治疗的两大瓶颈。因此,如何让CAR-T细胞“进得去”、“活得长”,是领域内亟需回答的重大科学问题。

生物力学是一门新兴交叉学科,由美籍华人物理学家Yuan -Cheng Fung(冯元桢)于上世纪60年代所创建。以往,人们主要是通过化学信号来理解生命的过程,而物理的力学信号则完全被忽略。近30年的研究证实,力学信号和化学信号共同决定了细胞的基本行为。如何利用力学信号解决人类疾病的问题是生物力学研究的基本目标。黄波团队早在2008年就开展生物力学在肿瘤和免疫领域的研究,采用软的纤维蛋白凝胶(弱的生物力学信号)实现肿瘤再生细胞(tumor-repopulating cell, TRC)凝胶内大量扩增 (Nat Mater. 2012;11:734-41)。进一步研究发现,TRC在硬的力学微环境中进入休眠状态( Cancer Res. 2018;78:3926-37.),而已分化的肿瘤细胞在弱的生物力学信号下能够进行逆分化,重新获得干性特征(Research. 2023:6:0215)。利用这种柔软性,团队自建方法将软的和硬的细胞进行分选,证实柔软性是干性细胞的基本特征(EMBO J. 2021;40:e106123.)。在应用层面,团队证实TRC利用其柔软性,通过机械变形有效吞噬载药囊泡,反而启动溶酶体途径将药物递送入核杀伤自身(Cell Res. 2016;26:713-27.),并揭示干性肿瘤细胞利用其柔软性逃避T细胞杀伤( Cancer Res. 2021;81:476-88.),而效应性T细胞则通过其柔软性避免自我杀伤的力学机制(Nat Commun. 2024;15:1405.)。在此基础上,团队黄波团队将CAR-T细胞种入纤维蛋白凝胶,利用生物力学信号,一方星空体育网站 星空体育首页面维持CAR-T细胞快速增殖,一方面阻断其分化,从而制备出庞大的干性CAR-T细胞群体,能够满足临床需求。
干性CAR-T扩增的背后折射出化学信号和生物力学信号本质性的区别。力学信号不仅有大小,而且有方向和频率,而化学信号仅有大小,没有方向和频率。令人吃惊的是,团队发现生物力学信号导致CAR-T细胞膜表面受体β2整合素胞内段出现磷酸化,而化学信号却无此作用。磷酸化的β2整合素一方面促使机械力感受蛋白YAP的磷酸化,同时募集14-3-3ζ蛋白诱发磷酸化的YAP走向降解。这一关键性分子事件解除了YAP对转录因子MafG的转录抑制作用,使得MafG得以表达,进而转录激活SOX2、NANOG等干性基因。与此同时,磷酸化的β2整合素将力学信号进行转导,激活MAPK信号通路,促进CAR-T细胞增殖,从而清楚阐释生物力学信号是如何将增殖程序和分化程序分开,使得CAR-T细胞 生长但不分化,并获得干性表型。
生物力学信号扩增的干性CAR-T在人肠癌,胶母细胞瘤以及胰腺癌患者来源的异种移植(PDX)小鼠模型中,均能够显著抑制肿瘤生长;更有意义的是,这种CAR-T制备周期短,无需额外添加因子且细胞用量低,必将极大降低CAR-T的使用费用。
黄波教授为论文通讯作者,课题组副研究员吕家迪、博士后王殿恒、博士生司甜为论文共同第一作者。中国医学科学院肿瘤医院张海增教授和郑州大学第一附属医院张毅教授,为本研究提供了临床样本和人源CAR-T质粒。
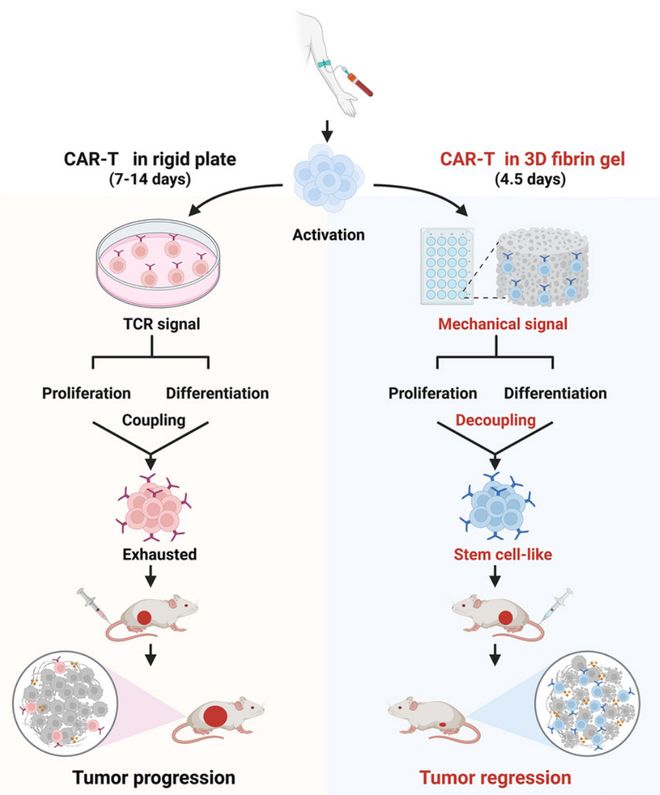
CAR-T细胞疗法在血液系统恶性肿瘤中已取得显著成功,但在实体瘤治疗中仍面临浸润不足、持久性差和易耗竭等核心瓶颈。黄波教授团队近期发表在Immunity期刊上的研究,创新性地利用3D纤维蛋白凝胶介导的生物机械力信号,成功实现了T细胞增殖与分化程序的“解偶联”,高效扩增出干性样CAR-T细胞,为破解实体瘤治疗困境提供了全新策略。
一是跳出了传统依赖化学信号调控的框架,首次揭示生物机械力信号可通过β2整合素–14-3-3ζ–YAP–MafG信号轴,激活包括SOX2、NANOG在内的干性基因网络,从而重塑T细胞功能调控的新范式;
二是所建立的制备工艺兼具“高效性”与“临床友好性”——仅需4.5天即可获得治疗剂量的干性样CAR-T细胞,用量减少50%,并显著降低细胞因子释放综合征风险,实现了“提质、增效、减毒”的多重优势,为实体瘤CAR-T疗法的临床转化奠定了坚实基础。
期待在更多类型的实体瘤模型中验证该技术的适用性,并在不久的将来加速其向临床治疗的推广应用。毋庸置疑,这项研究不仅为新一代CAR-T的设计提供了原创性工具,更通过生物力学与免疫学的深度融合,推动了细胞治疗领域的范式革新,展现出广阔的临床应用前景。
传统CAR-T疗法在血液肿瘤中势如破竹,却在实体瘤治疗中举步维艰。其核心瓶颈在于,体外扩增过程中T细胞发生了不可逆向耗竭状态分化,这些T细胞既无力穿透致密基质屏障,更难以在缺氧酸性的肿瘤微环境中持久作战。如何实现T细胞扩增与命运分化的”解”偶联(decoupling),赋予CAR-T细胞更强的浸润与杀伤能力,一直是CAR-T领域亟待解决的长期核心问题和研究热点。目前大量研究聚焦于T细胞受体(信号1)、共刺激分子(信号2)、细胞因子(信号3)及营养/代谢(信号4)等通路,但尚未取得显著突破。鉴于此,亟需开发能够实现增殖与分化解耦的关键技术,以在体外培养具备持续增殖能力的干细胞样CAR-T细胞。
中国医学科学院黄波团队独辟蹊径地引入生物力学维度,首次实现CAR-T细胞增殖与分化的精准解偶联。他们基于15年力学生物学积淀,创新性利用纤维蛋白凝胶的弱力学信号(0.5-1 kPa),仅用4.5天便规模化制备出具有干性特征的CAR-T细胞。这些细胞不仅保有强大的增殖活力,更展现出惊人的肿瘤浸润深度与长期驻留能力。尤为重要的是,团队揭示了力学信号通过β2整合素-YAP-MafG轴重塑细胞命运的分子机制:磷酸化的整合素如同“力学解码器”,既激活MAPK通路驱动增殖,又触发YAP降解释放MafG转录因子,最终激活SOX2/NANOG干性基因程序——这一机制完美诠释了“增殖而不分化”的内在机理。
这项研究展现出巨大的临床转化潜力,为癌症CAR细胞疗法的改进提供了极具前景的新策略:相较于传统化学因子诱导方法,力学调控的干性CAR-T制备周期缩短,细胞用量降低,且完全规避细胞因子风暴风险。在胰腺癌荷瘤小鼠模型中,该疗法显著提升了肿瘤的治疗效果,并且为胶质瘤等难治性实体瘤带来突破性希望。当然如何精准调控“力的剂量”(强度/频率/方向),确保其在人体微环境中的长效稳定性,仍需通过大规模临床试验验证。

【非原创文章】本文著作权归文章作者所有,欢迎个人转发分享,未经作者的允许禁止转载,作者拥有所有法定权利,违者必究。

特别声明:以上内容(如有图片或视频亦包括在内)为自媒体平台“网易号”用户上传并发布,本平台仅提供信息存储服务。
前苏联领袖赫鲁晓夫,拯救民众脱离苦难,被人民称作玉米狂魔
张靓颖发文自曝健康状况:营养不良,额头血管莫名突起,伸个懒腰手掌就流血了
英超BIG6本轮仅曼城&曼联无缘胜利,曼联开赛2轮最惨1平1负排第16
英伟达被曝 2026Q1 完成 Rubin GPU 所需 HBM4 12Hi 最终质量测试
联想拯救者回应 Y9000P 笔记本屏幕像哈哈镜:OLED 无法绝对平整

