对于荧光定量PCR的结果的判断,最直观的判断就是看扩增曲线是否正常。很多老师会遇到异常扩增曲线的困扰,接下来我们会结合几个实例,带着大家一起来看一下常见的异常扩增曲线
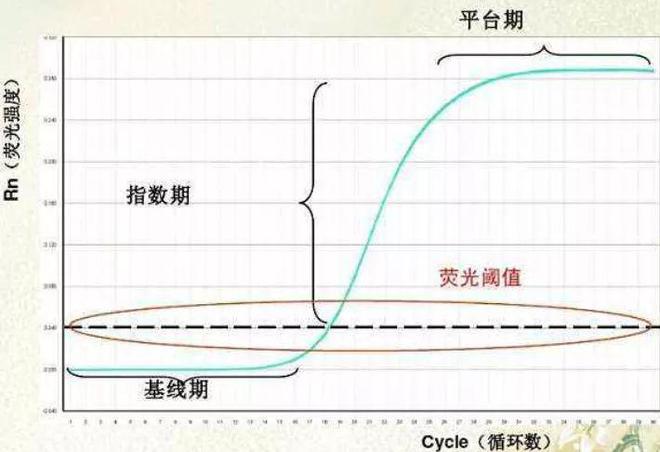
随着实验的进行,扩增产物不断累积,相应的荧光信号也不断在增加,每进行一个循环就采集一次荧光的信号,经过一定的循环数后(比如40个循环),就可以得到下面的扩增曲线图(横坐标代表扩增的循环数cycle,纵坐标代表荧光的强度)。
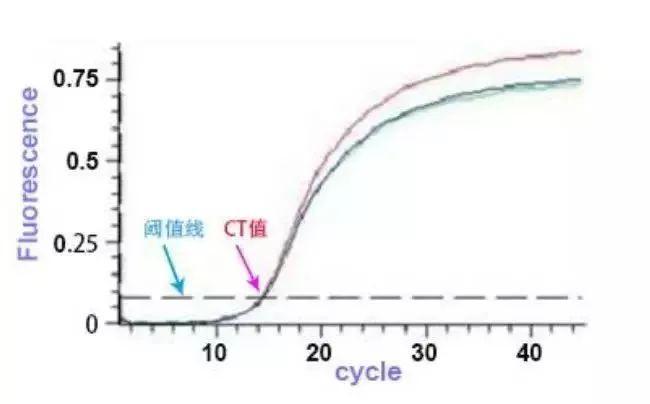
基线:指在PCR扩增反应的最初的几个循环里,荧光信号变化不大。接近一条直线,该直线叫做基线。这个了解即可,对实验操作没什么影响。
阈值线个循环的荧光信号作为荧光本底信号,阈值的设定就是3-15个循环荧光信号标准差的10倍,在PCR扩增的指数期(如图中箭头所指)。
说的这么严肃,其实很多仪器自动设定的阈值线基本能够满足我们的实验要求,不需要我们手动设置的。
CT值:我们常会用CT值来计算我们的相对含量,即扩增产物的荧光信号到达设定的阈值线时所经历的扩增的循环数,也就是图中扩增曲线和阈值线的交汇处的横坐标所显示的值。
做标准曲线有啥用?标准曲线可以用来确定未知的样品的初始量。如果是需要绝对定量,是必须要有标准曲线的。
怎么做呢?每个模板的CT值与该模板的起始的拷贝数的对数是存在线性关系的,起始的拷贝数越大,CT值就越小。标准品按照一定的倍数稀释5-6个浓度左右,根据RT-PCR的反应条件进行反应。以标准品拷贝数的对数值为横坐标,CT值为纵坐标,绘制线性曲线。而未知样品的拷贝数即可根据曲线方程计算得来。
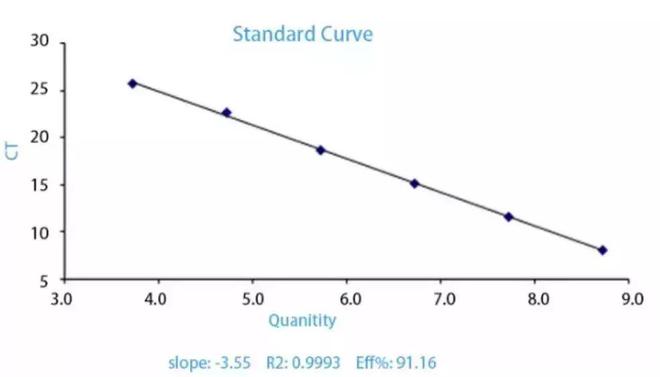
(1)如果是做绝对定量,标准品的要求比较高,这个的制备过程也相对复杂一些,但结果也更加精确。
必须是准确定量的、标准化的、稳定的质粒DNA(也可以是基因组DNA,纯化后的PCR产物等),
(2)如果只是想看看扩增效率(E)(E=10-1/斜率),检验PCR的反应体系是否符合要求,我们有时候也采用待测试样品作为标准品,逐步稀释后进行反应,最终看标准曲线
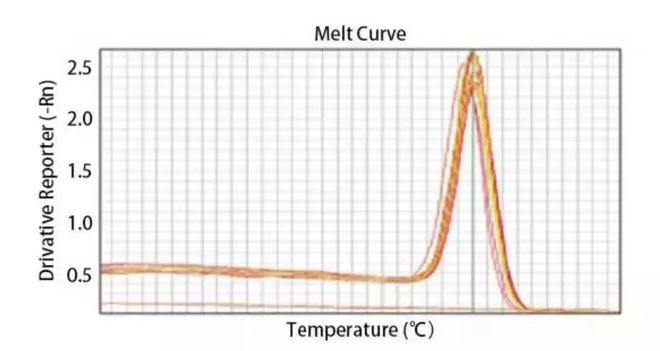
简单点说,就是考察染料标记法结果的特异性的。再简单点,就是分分钟确定你的引物是否有效。
复杂的原理就不解释了,关键是怎么看和怎么判断。如果反应产物单一,曲线会出现一个尖峰;如果有二聚体或者非特异性的扩增,就会出现至少两个峰或者更糟糕。采用SYBR Green染料时是必须要做溶熔解曲线的,毕竟这是一个非特异性的染料。
这种情况下很有可能是你的起始模板浓度太低了,即便经过40个循环也是达不到平台期的,可以通过增加循环数来验证是否是该问题。
(2)熔解曲线的问题:比如多个峰,或者尖峰的前面有个小小的小峰,或者没有峰?
这个跟引物以及反应的体系温度有关系,如果说没有峰值或者杂乱无章,很有可能是引物的问题,建议重新设计引物。有时候有小的峰,可以通过优化反应条件,比如退火温度的优化来消除这个影响。
对照试剂盒说明书,检查时间、温度、循环数、荧光采集等是否设置正确。有一个比较容易忽略的设置问题是,需要看下所选用的试剂中是否含有ROX来作为参比荧光染料。
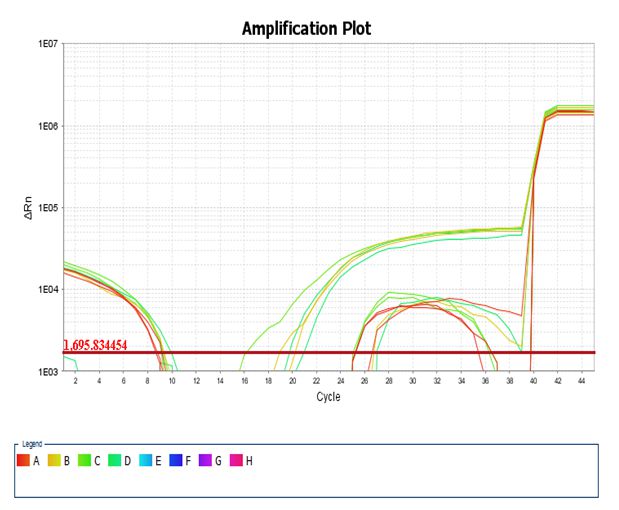
荧光定量PCR 仪加热模块分0.2ml跟0.1ml两种,如果0.1ml加热模块用成0.2ml耗材,则会造成耗材压扁,甚至造成机器故障;如果0.2ml加热模块用成0.1ml耗材,则会造成反应管的外壁和荧光定量PCR仪器的温控模块没有充分接触,从而出现热传导不充分,进而影响酶的活性,会引起重复性不好(图四),或者溶解曲线多峰(非特异扩增),甚至是假阴性结果;
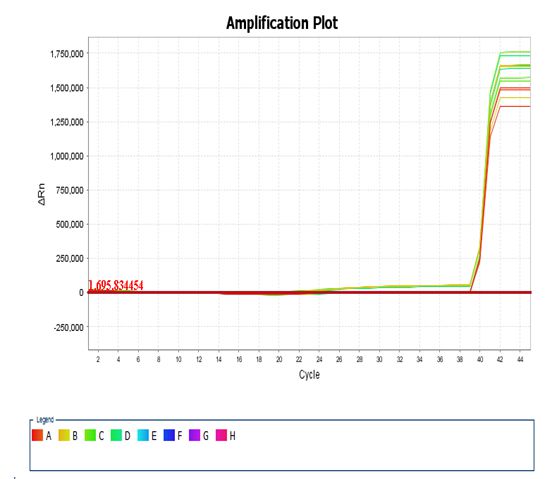
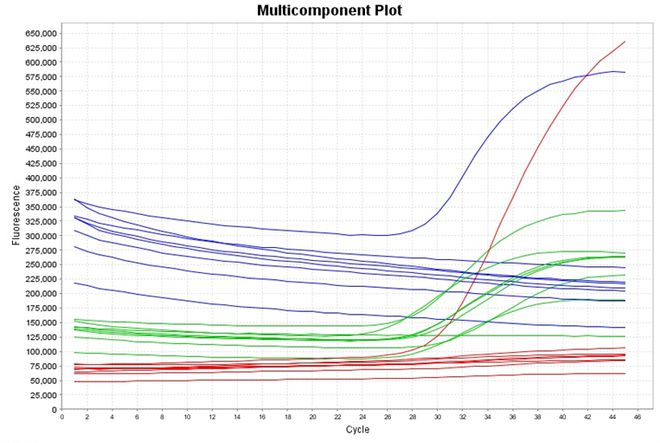
如果使用的PCR反应板封膜质量不好,在PCR过程中受到水蒸气的影响,容易产生变形(图星空体育网站 星空体育首页六),这样会引起“optical warping”,即“光学扭曲”现象(图七 左图),该实验中由于使用了ROX作为参比染料,ROX有效的校正了这种荧光信号的变化,均一化的扩增图结果是正常的。
除了耗材外,跟仪器配套使用的配件也要检查是否使用正确,比如配套的8联管托架,在使用的时候只用托架的下半部分,如果忘记把上半部分取下,有可能会影响扩增(图八)。
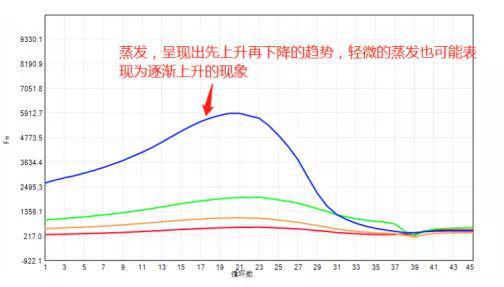
首先要确定试剂是否有效,包括查看试剂是否在有效期内,是否反复冻融多次,运输条件是否正常。可以通过比较试剂的批次号,结合实验中的阳性对照结果,确定试剂的有效性。其次要观察扩增完的试剂体积,如果在扩增过程中有试剂的蒸发,可能会引起扩增曲线抬升现象,如果实验体系中加入了ROX作为参比荧光,ROX荧光可以区分扩增曲线抬升是真扩增,还是蒸发。
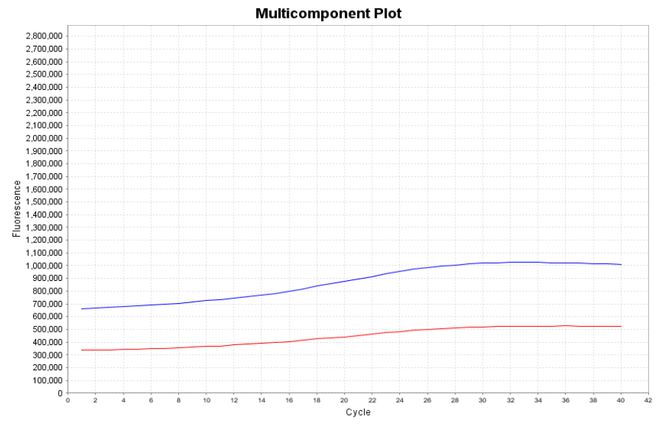
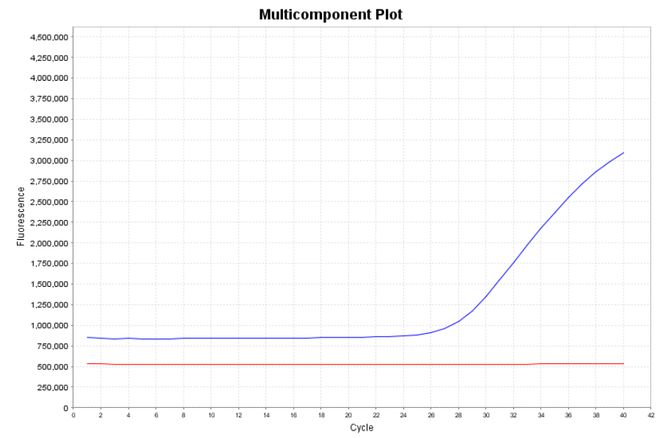
因为样本是水相会在上层,试剂(含有甘油成分)会在下层,在前期的PCR过程中不足以混匀完全,这样会形成折射,荧光较强,而一般加热几个循环后样本跟预混液会混匀,荧光就变稳定了(图十)。
手动设置基线。将Baseline End设置为“扩增信号出现的前一个循环”即,图片展原始为26,将其设置为20,点击OK即可恢复正常曲线:荧光定量PCR实验结果中无Ct值出现
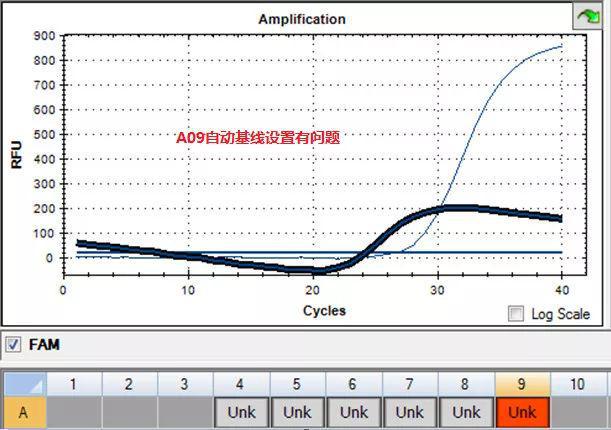
(3)引物或者探针降解:可通过PAGE电泳检测其完整性;(4)电脑设置了自动休眠。
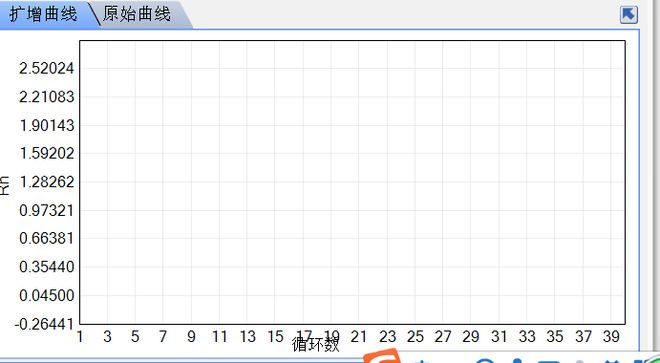
分液不准确,检查检测后的反应管可发现管内的PCR反应液量明显少于正常管;
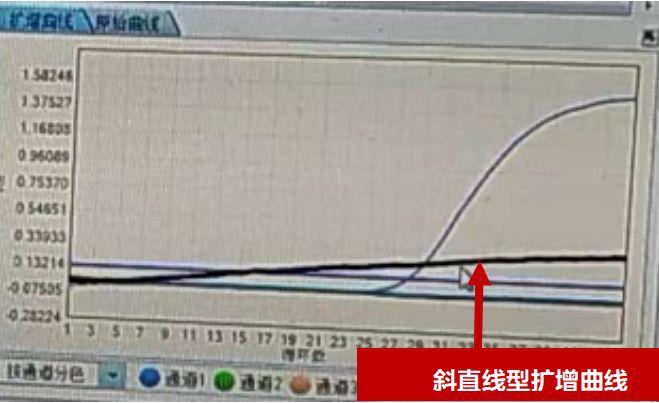
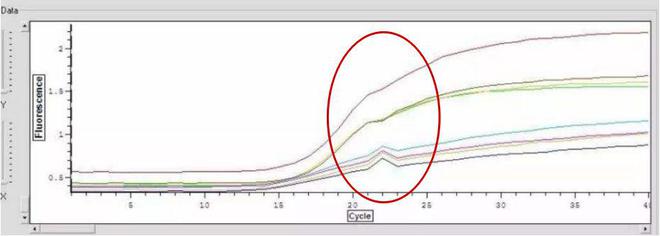
反应管气密性差,反应过程中溶液蒸发引起探针浓度增加,导致曲线呈斜直线状。
(2)复检样本,排除非特异性扩增的可能性;(3)正常样本也可存在曲线末尾起跳,表示样本浓度低或者加样量不准确。
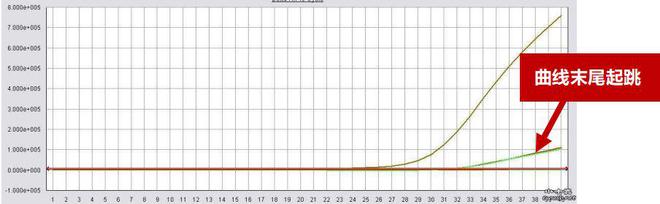
排除污染原因后复检样本,如果复检后曲线为阴性直线则说明之前的末尾起跳为非特异性扩增,如果复检后曲线仍与之前一致则说明末尾起跳表示该样本中待检病毒核酸的浓度偏低。
(2)如果尖峰向下,可能是卤素灯老化所致发射光源不稳定(指卤钨灯光源的激发器)
(3)如果是单一的孔位出现尖峰,除了考虑仪器或者孔位问题外,还要考虑反应体系是否有气泡所致。解决方案:
1.曲线拐点清楚,特别是低浓度样本指数期明显,扩增曲线整体平行性好,基线平而无上扬现象,低浓度样本扩增曲线.曲线指数期斜率与扩增效率成正比,斜率越大扩增效率越高。
3.标准的基线平直或略微下降,无明显的上扬趋势。4.各管的扩增曲线平行性好,表明各反应管的扩增效率相近。
新冠核酸检测过程中每一个环节的操作都有可能产生异常扩增曲线,干扰结果判读。检测人员在上岗前需完成操作培训和考核,在实际工作中严格遵循规范化流程,掌握专业知识,积累实践经验,才能保证新冠核酸的检测质量。

风信子亨廷顿舞蹈症关爱中心创始人曹茜因直肠癌去世,从确诊到去世仅50余天
酷比魔方掌玩 mini 3 Ultra 平板规格公布,国补后 1400 元
小米推出“米家中央空调 Pro 风管机 4 匹超一级能效”,7999 元
《编码物候》展览开幕 北京时代美术馆以科学艺术解读数字与生物交织的宇宙节律

