在肿瘤免疫中,CD8+T细胞的作用和转化较为成熟。相比较,CD4+T细胞的相关研究较为有限。尽管如此,CD4+T细胞与多种肿瘤的免疫治疗反应、过继T细胞疗法和疫苗的效果紧密相关 (详见BioArt报道:;;;;;) 。一方面,CD4+T细胞的扩增预测临床结局,且CD4+T细胞向Th1和Tfh分化有助于抗肿瘤免疫效果。另一方面,调节性T细胞 (regulatory CD4+T cell,。因此,虽然活化的CD4+T细胞是肿瘤免疫防线的重要组成,但影响CD4+T细胞抗肿瘤效果的机制仍然不清楚。

为了解CD4+T细胞反应的异质性,作者对人肾癌组织分离的PD1+CD45RA-CD4+T细胞行scRNA-seq分析。UMAP分析将PD1+CD45RA-CD4+T细胞分为3群:C1为Treg样,表达FOXP3和L2RA;C2为Th1样,表达TBX21、EOMES和细胞毒分子;C3则为干细胞样,其不表达任何谱系相关转录因子 (lineage-negative,Lin-) ,如BCL6、TBX21、GATA3或RORC,而表达TCF7和干细胞样基因,同时富集干细胞样CD8+T细胞特征基因,表明一种静息状态。流式分析也证实这三种细胞群在肾癌、膀胱癌和前列腺癌存在,表明并不是肾癌独有现象。在肿瘤相关淋巴结中,作者同样发现在PD1+CD45RA-活化CD4+T细胞中,20-60%是TCF1+Lin-的干细胞样细胞群,表明在多种肿瘤组织和淋巴结中TCF1+Lin-是活化CD4+T细胞的主要群体。随后,作者发现TCF1+Lin-CD4+T细胞可以在体外增殖并向Th1、Treg和Tfh亚群分化。另外scRNA-seq和scTCR-seq分析表明肾癌组织内TCF1+Lin-CD4+T细胞和其他Treg等亚群的TCR有重叠,表明这些细胞存在谱系关系。这些结果说明TCF1+Lin-CD4+T细胞具有干细胞样特征并作为前体细胞进一步分化为效应细胞亚群。
紧接着,作者使用表达LCMV糖蛋白 (glycoprotein,GP) 的TRAMPC1细胞接种小鼠以在体内监测抗原特异性TCF1+Lin-CD4+T细胞的功能和分化动力学。在第星空体育 星空体育平台一周,GP66+CD4+T细胞在淋巴结迅速扩增并持续存在,且已经出现TCF1+Lin-CD4+T细胞群。5周后,淋巴结内GP66+CD4+T细胞存在TCF1+Lin-、Foxp3+和Bcl6+群,以及小部分Tbet+和RORγt+细胞群。在肿瘤内,大部分GP66+CD4+T细胞为Treg样,小部分为TCF1+Lin-。之后,作者将从SMARTA小鼠 (表达LCMV GP特异性TCR) 分离的初始CD4+T细胞过继入TRAMPC1细胞接种的小鼠,同样发现类似的分化轨迹。与此同时,分离TRAMPC1细胞接种小鼠淋巴结的TCF1+Lin-CD4+T细胞并过继入正常小鼠后给予LCMV感染,发现大部分过继细胞分化为Th1和Tfh细胞,小部分为Treg,表明TCF1+Lin-CD4+T细胞的分化亚群方向取决于所处环境。总之,这些结果进一步说明TCF1+Lin-是一种干细胞样CD4+T细胞。
前述结果表明肿瘤及其淋巴结Treg占PD1+CD4+T细胞主要群体,作者猜想Treg是否抑制TCF1+Lin-CD4+T细胞向其他效应亚群分化。Foxp3-DTR小鼠结合TRAMPC1细胞接种实验证实Treg缺陷后GP66+CD4+T细胞显著扩增且向Th1分化,且非抗原特异性CD4+T细胞也向Th1分化。scRNA-seq表明Treg缺失时,TCF1+Lin-CD4+T细胞在保留干细胞基因同时上调Th1相关基因表达。TCR-seq进一步证实Treg缺失促进的Th1细胞与TCF1+Lin-CD4+T细胞的TCR存在90%重叠,表明TCF1+Lin-CD4+T是Th1细胞的前体细胞。随后,作者分选TRAMPC1细胞接种小鼠的SMARTA干细胞样细胞或Treg细胞后过继入WT或Foxp-DTR小鼠,2天后白喉毒素处理。5天后分析发现,WT小鼠内过继的干细胞样细胞在淋巴结存在,小部分向Treg和Tfh分化;而Treg缺失时,过继的干细胞样细胞大量分化为Th1细胞。过继的SMARTA Treg则无论Treg是否敲除均保留Foxp3表达。这些结果说明TCF1+Lin-细胞在肿瘤中可以向Th1分化,但能被Treg抑制。
那么这种TCF1+Lin-CD4+T细胞来源的Th1细胞分化对抗肿瘤免疫是否有用?作者在TRAMPC1-GP 和B16F10-GP两种肿瘤模型中发现,CD4+T细胞删除削弱抗肿瘤免疫,且CD4+T细胞的作用依赖于CD8+T细胞。CD4+T细胞删除引起淋巴结干细胞样CD8+T细胞扩增但效应分化显著降低,而Treg删除则可以促进CD8+T细胞效应分化和扩增,提示干细胞样CD4+T细胞或Th1细胞诱导淋巴结CD8+T细胞的效应功能。为了厘清哪种细胞起作用,作者在SMARTA T细胞中构建四环素诱导的TBET过表达荷瘤小鼠内。相比于对照组,四环素诱导联合PDL1抑制剂有效促进CD4+T细胞的Th1分化以及CD8+T细胞的扩增和效应分化,并展现良好的肿瘤控制,表明Th1亚群促进CD8+T细胞的效应分化。相反,当作者在四环素TBET过表达的 SMARTA T细胞中敲除IFNγ时,上述TBET过表达介导的CD4+/CD8+T细胞效应分化和抗肿瘤效应消失。同样,缺失Ifngr1的CD8+T细胞不再对CD4+T细胞反应。最后,作者在人肾癌组织中发现Th1细胞频率与效应CD8+T细胞浸润以及肿瘤免疫抑制剂治疗效果正相关。
这些结果均表明Th1细胞分泌的IFNγ在诱导CD8+T细胞抗肿瘤中的重要作用。
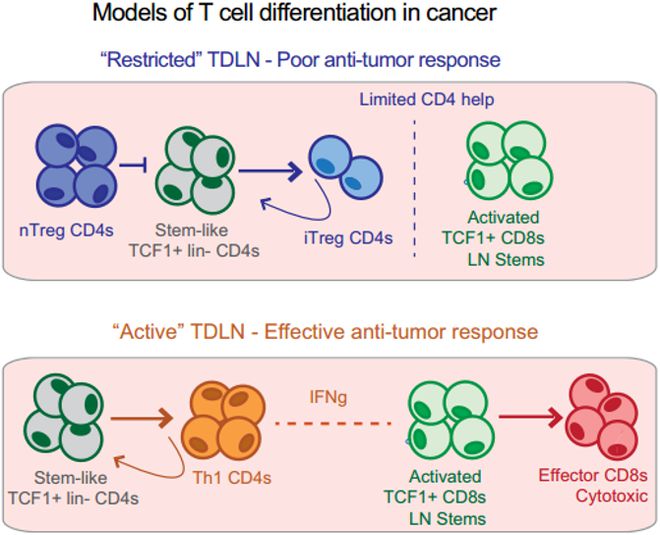
综上所述,这项研究揭示肿瘤特异性TCF1+Lin-干细胞样CD4+T细胞具有增殖和分化能力,其分化亚群方向对CD8+T细胞的抗肿瘤免疫起到重要作用,为靶向CD4+T细胞的肿瘤免疫疗法提供理解和应用思路。
【原创文章】BioArt原创文章,欢迎个人转发分享,未经允许禁止转载,所刊登的所有作品的著作权均为BioArt所拥有。BioArt保留所有法定权利,违者必究。
特别声明:以上内容(如有图片或视频亦包括在内)为自媒体平台“网易号”用户上传并发布,本平台仅提供信息存储服务。
做不完,根本做不完!杭州500米巷子卖出10万多只!没人能空手走出去...
太滑稽了!外网有人指责哈尔滨人:冬天疯狂采冰,破坏生态环境,导致夏天无冰可采
韩综“年终总结”,意外爆出具俊晔线岁唐国强近照,老到认不出,走路小心翼翼
综合续航超1400km 奇瑞风云T11首台PT车下线 PLUS中型SUV 外观内饰均升级
不止5G基带!苹果押注自研:iPhone 17系列将首发蓝牙和Wi-Fi芯片

