CAR-T细胞疗法是一种免疫疗法,通过改造患者自身的T细胞,使其能够识别并攻击癌细胞。然而,这种疗法的主要限制之一是这些细胞在体内的持续时间较短。研究表明,CAR-T细胞中与记忆相关的基因表达与其在患者体内的长期持续和临床疗效有关,这暗示记忆程序可能是持久CAR-T细胞功能的基础。
相反,FOXO1的过表达诱导了与T细胞记忆一致的基因表达程序,并在FOXO1结合基序上增加了染色质的可及性。过表达FOXO1的CAR-T细胞在长期刺激的环境中保留了它们的功能、记忆潜力和代谢适应性,并在体内展示了增强的持续存在和肿瘤控制能力。
因此,通过过表达FOXO1可以增加人类CAR-T细胞的抗肿瘤活性,并强调了记忆重编程作为一种广泛适用的方法,在优化治疗性T细胞的状态具有重要作用。

文献中通过使用FOXO1的小分子抑制剂(FOXO1i)和CRISPR-Cas9基因编辑技术敲除FOXO1(FOXO1KO),研究了FOXO1对CAR-T细胞功能的影响。结果显示,FOXO1的抑制或敲除导致了CAR-T细胞的记忆相关基因表达下降,如CD62L、IL-7Rα和TCF1等,同时促进了疲劳相关基因的表达,如CD39、TIM-3和TOX。
这种基因表达的变化导致了CAR-T细胞功能的损害,包括减少的扩增能力、降低的CD8+ T细胞频率,以及减弱的抗肿瘤活性。这些结果表明,内源性FOXO1对于维持CAR-T细胞的记忆状态和抗肿瘤功能至关重要。
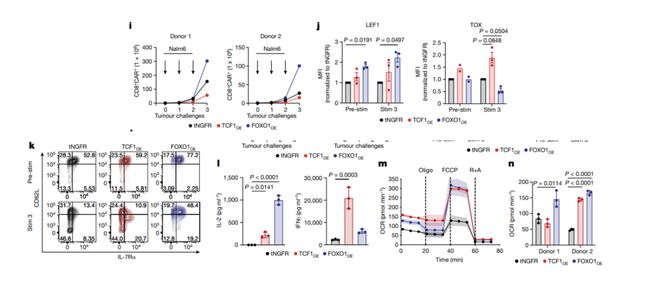
为了进一步研究FOXO1的作用,研究者通过过表达FOXO1来增强其在CAR-T细胞中的活性。结果显示,过表达FOXO1的CAR-T细胞表现出了增强的记忆相关基因表达,并且即使在长期刺激的条件下也能保持其功能和记忆潜力。
更重要的是,这些细胞在体内的持久性和抗肿瘤能力得到了显著提升。在小鼠的白血病模型中,与对照组相比,过表达FOXO1的CAR-T细胞显示出更长的生存时间和更有效的肿瘤控制。
这些发现表明,通过调节FOXO1的活性,可以优化CAR-T细胞的治疗潜力,使其在体内更有效地持久和抗肿瘤。
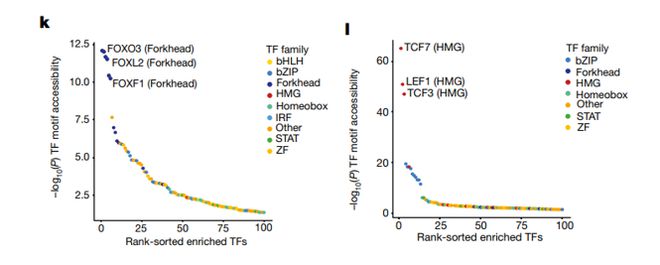
研究中比较了FOXO1和TCF1(由TCF7编码)在CAR-T细胞中的作用。尽管TCF7与CAR-T细胞记忆程序有关,但研究发现,过表达TCF1并没有强制执行规范的记忆程序或增强CAR-T细胞的效力。相比之下,FOXO1的过表达诱导了与T细胞记忆一致的基因表达程序。
为了确定 FOXO1 是否也能提高 CAR-T 细胞对实体瘤的活性,科学家通过将 tNGFR 或 FOXO1OE HER2.BBζ CAR-T 细胞注入 143B 骨肉瘤 NSG 小鼠体内。与白血病模型一致,FOXO1OE 细胞表现出持久的抗肿瘤活性和持续性。
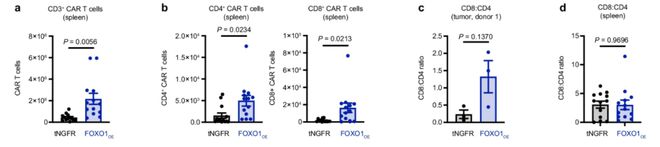
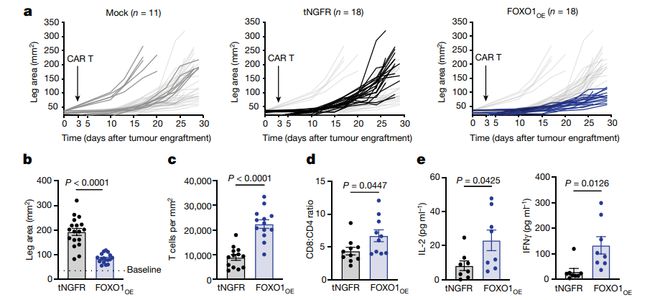
这些数据表明,FOXO1OE 以一种不依赖于 TCF7 的方式增加了 CAR-T 细胞在体内的扩增、持续性和肿瘤控制,而 TCF1OE 则没有提供可衡量的益处。
FOXO1OE 介导的增强依赖于 DNA 结合和核输出,这表明核穿梭介导的调整或信号调节对于有效的 FOXO1 介导的记忆编程非常重要。
FOXO1靶基因,包括TCF7,在输注前介导患者临床反应的CAR-T细胞中富集,这就提出了一种可能性,即内源性 FOXO1 活性可能预示着临床 CAR-T 产品具有强大的抗肿瘤活性。
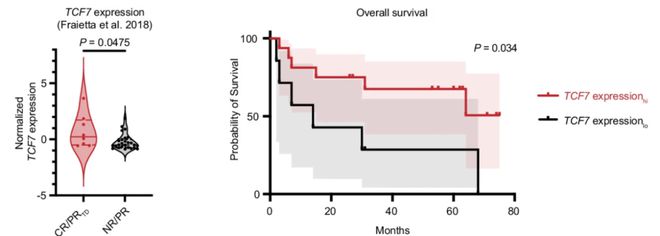
然而矛盾的是,在CLL成人患者中,灌注前 CD19.BBζ 细胞中的 FOXO1 转录水平与治疗反应或存活率无关。这是由于 FOXO1 主要是翻译后调控而不是转录调控。
团队通过假设 FOXO1 靶基因的总体表达可以更好地接近 FOXO1 的活性。基于此发现了一个由 41 个重叠 DEGs 组成的 FOXO1 调控子,这些 DEGs 在 FOXO1KO 细胞中下调,而在 FOXO1OE 细胞中上调。
与 FOXO1 转录物不同的是,FOXO1 调控子在 CLL 患者的灌注前 CAR-T 细胞中显著富集,这些患者表现出完全或部分应答,疾病也发生了转化,并且与体内 CAR-T 细胞扩增和总存活率有关。
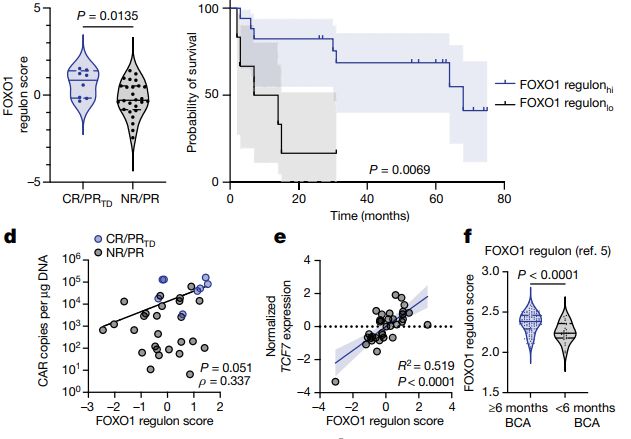
另外,在B细胞急性淋巴细胞白血病(B-ALL)患儿的预制造效应T细胞中也富集了FOXO1调控子,这些效应T细胞表现出持久的CAR-T细胞持久性,支持了FOXO1活性与CAR-T细胞疗效广泛相关的观点。
研究结果表明,通过过表达FOXO1可以增加CAR-T细胞的抗肿瘤活性,并强调记忆重编程作为一种广泛适用的方法,用于优化治疗性T细胞的状态。
研究者也提出了未来研究的方向,包括进一步探索FOXO1和TCF1在人类工程化和非工程化T细胞中的作用,以及FOXO1在其他免疫疗法中的潜在相关性。

